Memoria immunitaria innata e adattiva: un continuum evolutivo nella risposta dell'ospite ai patogeni (parte 1)
Jun 08, 2022
Per saperne di più info contattacidavid.wan@wecistanche.com
Memoria immunologicaè un importante tratto evolutivo che migliora la sopravvivenza dell'ospite dopo la reinfezione, la memoria è una caratteristica riconosciuta sia nel braccio innato che in quello adattivo del sistema immunitario. Sebbene i meccanismi e le proprietà attraverso cui vengono indotti la memoria immunitaria innata e adattativa siano distinti, essi colludono per migliorare la difesa dell'ospite contro i patogeni. Qui, proponiamo che la memoria immunitaria innata, o "immunità allenata", sia una forma primitiva di adattamento nella difesa dell'ospite, risultante dalla riorganizzazione della struttura della cromatina, che fornisce una risposta aumentata ma non specifica alla reinfezione. Al contrario, la memoria immunitaria adattativa è più avanzata, con una maggiore ampiezza della risposta mediata da cambiamenti epigenetici, nonché specificità mediata daricombinazione genica. Un modello integrativo della memoria immunitaria è importante per un'ampia comprensione della difesa dell'ospite e per identificare gli approcci più efficaci per modularla a beneficio dei pazienti con infezioni e malattie immuno-mediate.

Clicca qui per saperne di più su Cistanche
Immunità innata e adattativa
Classicamente, l'immunità dell'ospite è divisa in risposte immunitarie innate e adattative. Il primo reagisce rapidamente e in modo non specifico ai patogeni, mentre il secondo risponde in modo più lento ma specifico, con la generazione di una memoria immunologica di lunga durata (Farber et al., 2016). Questa dicotomia ha dettato l'ultimo mezzo secolo diricerca immunologicae un vasto numero di studi ha definito i substrati cellulari e molecolari di ciascuno di questi due componenti principali della difesa dell'ospite. L'immunità innata è mediata da popolazioni di cellule immunitarie innate come cellule mieloidi, cellule natural killer (NK) e cellule linfoidi innate (ma anche cellule non immuni in circostanze specifiche), nonché da antichi sistemi umorali come defensine e complemento . L'immunità adattativa è un tratto evolutivo relativamente nuovo basato sulla famiglia delle immunoglobuline e su cellule come i linfociti B e T nei vertebrati mascellari (Danilova, 2012) e sui recettori dei linfociti variabili (VLR) costituiti da segmenti ricchi di leucina ripetuti (LRR) nei vertebrati senza mascelle (Boehm et al., 2012).
Durante un'infezione, l'immunità innata è la prima ad essere attivata (la reazione infiammatoria), che impiega non più di minuti o ore per essere completamente attivata (Netea et al.,2017). Questo è fondamentale per la difesa dell'ospite nella prima fase di una nuova infezione. Sebbene l'immunità innata sia generalmente in grado di eliminare i patogeni in modo efficiente, l'eliminazione iniziale dell'infezione può fallire a causa dell'alto numero o della virulenza diagenti patogeni invasori. In queste situazioni si attivano i linfociti e i meccanismi immunitari adattativi, che consentono il riconoscimento e l'eliminazione specifici del patogeno. L'instaurazione dell'immunità adattativa richiede 1-2 settimane ed è importante per la difesa dell'ospite durante le ultime fasi dell'infezione e durante le infezioni secondarie a causa della sua capacità di "ricordare" e rispondere in modo più efficace alla restimolazione (Farber et al.,2016) .
I processi immunitari innati e adattativi erano inizialmente visti come risposte relativamente compartimentate nel tempo, ma la ricerca negli ultimi due decenni ha chiaramente dimostrato forti legami e una rete efficiente tra di loro. L'attivazione della risposta immunitaria adattativa e l'induzione della memoria immunitaria classica nei linfociti dipendono dal sistema immunitario innato, in particolare dalle cellule che presentano l'antigene come le cellule dendritiche. Gli effetti a valle dell'attivazione dei linfociti vengono quindi esercitati amplificando le risposte immunitarie innate come la fagocitosi e l'uccisione di agenti patogeni da parte di alcune cellule immunitarie innate. Due proprietà che discriminano tra immunità innata e adattativa sono da un lato la specificità e dall'altro la capacità di costruire una memoria immunologica di lunga durata. Le risposte immunitarie innate sono tradizionalmente ritenute aspecifiche e prive della capacità di adattamento, mentre le risposte immunitarie adattative riconoscono con grande precisione diversi patogeni utilizzando processi di ricombinazione genica nella famiglia dei geni delle immunoglobuline e successivamente costruiscono la memoria immunologica (Danilova, 2012) (Figura 1). Il concetto che l'immunità innata non è specifica è stato messo in discussione dalla scoperta dei recettori di riconoscimento del modello (PRR). Questi recettori espressi su una varietà di cellule all'interno del sistema immunitario innato riconoscono componenti specifici dimicrorganismi, e la combinazione di PRR espressi da una cellula immunitaria può portare a un riconoscimento parzialmente specifico del tipo di microrganismo incontrato: ad esempio, le cellule immunitarie innate riconoscono la differenza tra un batterio Gram-negativo e un Gram-positivo, ma non tra due strettamente specie o ceppi correlati (Medzhitov e Janeway, 2000). In questa recensione non discuteremo i progressi nella comprensione del riconoscimento del patogeno attraverso i PRR, poiché questo è oggetto di molte eccellenti revisioni recenti in letteratura (ad es. O'Neill et al., 2013).

Figura 1. Risposte immunitarie innate e adattive
Durante le prime ore e giorni di infezione, l'invasione da parte di agenti patogeni induce l'attivazione di cellule immunitarie innate come macrofagi, monociti o cellule NK o fattori umorali come il complemento. Questi percorsi attivano fortemente una reazione infiammatoria ed eliminano i patogeni (immunità innata). Nei pochi casi in cui l'infezione non viene eliminata, i patogeni vengono ingeriti ed elaborati dalle cellule presentanti l'antigene, seguiti dalla presentazione dell'antigene e dalla stimolazione dell'attivazione specifica diLinfociti T e B. A sua volta, questo porta all'espansione clonale e all'attivazione di meccanismi effettori (p. es., il rilascio di citochine e immunoglobuline) (immunità adattativa).
Qui, ci concentreremo sulla seconda proprietà che discrimina i meccanismi di difesa innati e adattativi dell'ospite: l'induzione della memoria immunitaria. In contrasto con la prima letteratura, un numero crescente di prove mostra che le risposte immunitarie innate mostrano caratteristiche adattive (Bowdish et al.,2007; Netea et al.,2011). Nelle piante e negli invertebrati privi di immunità adattativa, è stata segnalata una protezione prolungata contro la reinfezione (Kurtz, 2005). Studi sui mammiferi hanno dimostrato che esiste una protezione crociata contro infezioni con diversi patogeni (Quintin et al, 2014), mentre studi sperimentali su topi privi di cellule immunitarie adattive funzionali hanno mostrato una protezione parziale in alcuni modelli di vaccinazione (Bistoni et al., 1986; impossibile Wout et al, 1992). È quindi evidente che l'immunità innata può essere modulata da precedenti incontri con microbi o prodotti microbici, e questa proprietà è stata definita "immunità allenata" e rappresenta di fatto una memoria immunitaria innata.
Tuttavia, esistono meccanismi molecolari distinti che mediano i due tipi di memoria immunitaria. Sulla base di argomenti molecolari, immunologici ed evolutivi, proponiamo che la memoria immunitaria innata sia una forma primitiva di memoria immunitaria presente in tutti gli organismi viventi, mentre la memoria immunitaria adattativa è una forma avanzata di memoria immunitaria che rappresenta un'innovazione evolutiva nei vertebrati. Sulla base delle proprietà complementari dei due tipi di memoria immunitaria e su una serie di argomenti biologici come descritto di seguito, sosteniamo in questa prospettiva che lo sviluppo della memoria immunitaria innata e adattativa rappresenta un continuum evolutivo. Proponiamo inoltre che queste due forme siano due passi evolutivi verso lo sviluppo di meccanismi efficaci di adattamento a un ambiente ricco di potenziali patogenimicrorganismi.
La memoria immunologica come tratto evolutivo adattativo
Il dogma secondo cui la memoria immunologica è confinata al sistema immunitario adattativo affronta una difficoltà concettuale se considerata da una prospettiva evolutiva. Che la memoria immunitaria sia vantaggiosa da un punto di vista evolutivo è ben illustrato da antiche malattie mortali come il vaiolo: mentre la mortalità era storicamente del 20 percento -60 percento per le prime infezioni, in seguito gli individui sono diventati completamente immuni alla malattia (Riedel, 2005 ). Pertanto, è difficile immaginare che la memoria immunitaria si sia evoluta solo nei vertebrati, che rappresentano circa l'1% -2 per cento delle specie viventi (Gourbal et al.,2018). Al contrario, altri importanti tratti vantaggiosi, come la vista, si è evoluto indipendentemente più volte durante l'evoluzione di vari gruppi di animali (la cosiddetta "evoluzione convergente") (Gehring, 2004). È interessante notare chememoria immunologicaall'interno del lignaggio dei vertebrati si è evoluto non solo una, ma due volte. In primo luogo, lo sviluppo della memoria basata su VLR nei pesci senza mascelle (come la lampreda) e, in secondo luogo, lo sviluppo della memoria basata su LG (che è anche la base per lo sviluppo della memoria dei linfociti B e T) in tutti gli altri vertebrati mascellari. Che ci siano due eventi separati che portano alla memoria immunitaria nei vertebrati (Cooper e Alder, 2006), mentre sono completamente assenti in tutti gli altri metazoi, è molto improbabile.
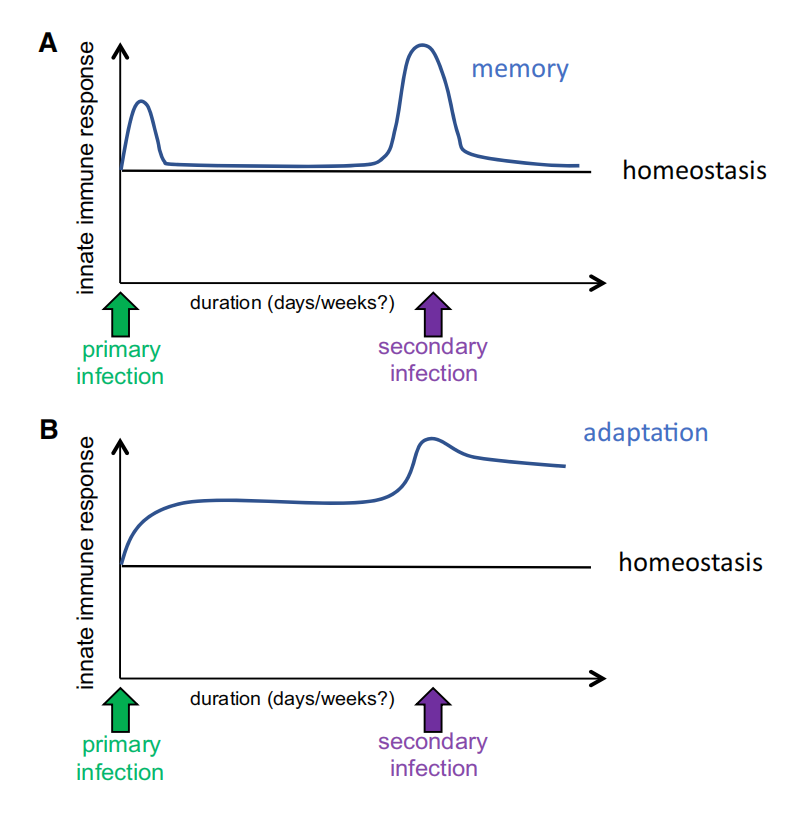
Figura 2. Memoria immunitaria contro adattamento immunitario
La memoria immunitaria è definita come uno stato modificato del sistema immunitario di un ospite dopo un'infezione acuta (o vaccinazione), che porta a una risposta più efficace contro la reinfezione. È importante sottolineare che durante l'induzione della memoria immunitaria, tra la prima infezione e la reinfezione, lo stato immunitario torna funzionalmente a uno stato basale basso, mentre la capacità di rispondere più forte alla restimolazione è impressa a livello epigenetico (A). Al contrario, l'adattamento è definito come il cambiamento a lungo termine della risposta immunitaria determinato da un cambiamento costante delle condizioni ambientali, o dovuto ad un insulto cronico (es. un'infezione cronica), che porta ad un nuovo stato funzionale. È importante sottolineare che lo stato immunitario funzionale durante l'adattamento non ritorna allo stato basale basso esistente prima dell'insulto (B).
In linea con ciò, un gran numero di studi di immunologia vegetale ha dimostrato che la difesa dell'ospite vegetale include caratteristiche adattive, una risposta denominata Systemic Acquired Resistance (SAR)(Jaskiewicz et al.,2011; Kachroo e Robin,2013; Reimer-Michalski e Conrath, 2016). I meccanismi molecolari e i mediatori biochimici della SAR sono ampiamente conosciuti (Kachroo e Robin, 2013), con il ricablaggio epigenetico della difesa dell'ospite che si suggerisce di svolgere un ruolo centrale (Luna e Ton, 2012). Inoltre, prove crescenti hanno sfidato il convinzione che l'immunità innata degli invertebrati manchi di tratti di memoria (Kurtz, 2005). Le proprietà adattative delle risposte immunitarie innate sono state riportate in diversi lignaggi di invertebrati; per esempio, ilmicrobiotaha dimostrato di indurre la memoria immunitaria innata per proteggere le zanzare dal plasmodio (Rodrigues et al, 2010) e l'insetto sociale Bombus Terrestris per mostrare la memoria immunitaria innata contro tre diversi agenti patogeni (Sadd e Schmid-Hempel, 2006) e la tenia Schistocephalus solidus per indurre memoria nel crostaceo copepode (Kurtz e Franz, 2003) e la memoria immunitaria innata è un meccanismo di difesa nelle lumache (Pinaud et al, 2016). Questi studi sono stati integrati da dati sui vertebrati che dimostrano che è possibile indurre una protezione parziale dalla reinfezione in modelli murini sperimentali anche in assenza di risposte immunitarie adattative funzionali (Bistoni et al.,1986; can't Wout et al.,1992 ). Inoltre, studi epidemiologici hanno mostrato una protezione eterologa da parte dei vaccini umani contro un ampio spettro di infezioni (Benn et al.,2013), con meccanismi probabilmente indipendenti dalle classiche risposte immunitarie adattative. Pertanto, è ragionevole concludere che la memoria immunologica può essere trovata non solo nei vertebrati ma anche nelle piante e negli animali inferiori (Kurtz, 2005; Ne-tea et al., 2011) che non ospitano un sistema immunitario adattativo classico.

Memoria immunitaria innata e adattiva: un processo evolutivo
Se questi dati sostengono fortemente la presenza della memoria immunitaria in tutti i gruppi di organismi superiori, come si può definirla? Una definizione semplice è che la memoria immunologica si riferisce alla capacità del sistema immunitario di rispondere più rapidamente ed efficacemente a un agente patogeno. Questa definizione comprende tutti i processi descritti come memoria immunitaria in piante, invertebrati e vertebrati, sebbene non discrimini tra le differenze nell'azione osservate all'interno dei vari gruppi di organismi. In una recente recensione, Pradeu e Du Pasquier (2018) propongono un modello multidimensionale di memoria immunitaria, in cui discriminano non meno di sei varietà di memoria immunitaria: memoria adattativa classica nei vertebrati, memoria immunitaria delle cellule NK, immunità allenata nelle cellule mieloidi , priming negli invertebrati, memoria immunologica nelle piante (ad es. SAR) e memoria basata su Crispr/Cas in batteri e archaea (Pradeu e Du Pasquier, 2018). Queste forme di memoria immunologica differiscono nelle loro proprietà in base a una serie di caratteristiche di base della risposta: forza, velocità, estinzione (inversione allo stato basale), durata e specificità. Tuttavia, sebbene questa classificazione sia utile per comprendere la presenza onnipresente della memoria immunitaria in tutti gli organismi viventi, riteniamo che questacompartimentazionedella memoria immunitaria non riflette il comune substrato molecolare, biologico e funzionale delle caratteristiche della memoria in diversi organismi.
In questa prospettiva, proponiamo un modello unificante di memoria immunitaria che si basa su due concetti:
C'è una differenza concettuale tra due forme di adattamento immunitario: la memoria immunitaria e la differenziazione immunitaria.
Un continuum evolutivo collega la memoria immunitaria innata e adattativa.
Il primo concetto da definire è rappresentato dalla differenza tra memoria immunitaria e adattamento immunitario. Definiamo la memoria immunitaria come uno stato modificato del sistema immunitario di un ospite dopo un'infezione acuta (o vaccinazione), che porta a una risposta più efficace contro la reinfezione. È importante sottolineare che durante l'induzione della memoria immunitaria, tra la prima infezione e la reinfezione, lo stato immunitario torna funzionalmente a uno stato basale basso, mentre la capacità di rispondere più forte alla restimolazione è impressa a livello epigenetico (Figura 2A). Al contrario, definiamo la differenziazione immunitaria come una forma di adattamento attraverso cambiamenti a lungo termine nel programma funzionale di un sistema (compresa la risposta immunitaria), determinata da un cambiamento costante delle condizioni ambientali o dovuta ad un insulto cronico (es. infezione), portando a un nuovo stato funzionale. È importante sottolineare che lo stato immunitario funzionale durante la differenziazione non ritorna allo stato basale basso esistente prima dell'insulto (Figura 2B). Esistono molte situazioni biologiche caratterizzate dall'adattamento attraverso la differenziazione immunitaria: una di queste situazioni può essere indotta ad esempio da cambiamenti stabili nel microbiota intestinale, noto per indurre effetti a lungo termine sulle risposte immunitarie locali. Il processo di differenziazione immunitaria è oggetto di molte altre eccellenti recensioni e non sarà al centro di questa Prospettiva.
Un'altra importante distinzione da fare è tra adescamento e memoria. L'adescamento è anche un termine che è stato utilizzato per descrivere l'aumento delle risposte a uno stimolo secondario, tuttavia, questo è spesso un processo acuto che non comporta effetti sulla memoria a lungo termine. Ad esempio, durante l'infezione acuta da malaria, c'è una nota iper-reattività delle cellule immunitarie ai microrganismi Gram-negativi che può portare a gravi sintomi acuti: le cellule immunitarie sono preparate a rispondere in modo acuto con un rilascio di citochine più elevato. Tuttavia, ciò non implica una risposta della memoria che persisterebbe per mesi o anni.
Qui, ci concentreremo sul concetto di memoria immunitaria, che crediamo caratterizzi tutti gli organismi viventi. Proponiamo che esista un continuum evolutivo tra memoria immunitaria innata e adattativa basato su due proprietà fondamentali mediate da meccanismi distinti:
● Aumento dell'ampiezza e della cinetica del re-
risposte alla reinfezione, che è mediata da processi epigenetici e caratterizza la memoria immunitaria sia innata che adattativa (presente in tutti gli organismi)
● Specificità delle risposte mnemoniche, mediate dal gene
ricombinazione, una proprietà specifica della memoria immunitaria adattativa (descritta fino ad ora solo nei vertebrati)

Memoria immunitaria innata
Mentre nell'immunità dei vertebrati è stato a lungo ipotizzato che le risposte immunitarie innate non possano adattarsi dopo un'infezione e, dopo la reinfezione, ogni volta viene suscitata una risposta identica, questa ipotesi non è mai stata seguita nelle piante o nell'immunità degli invertebrati. Oltre agli studi sulle piante e sulle difese dell'ospite invertebrati descritti sopra (vedi Memoria immunologica come tratto evolutivo adattivo), sono stati proposti diversi meccanismi per spiegare l'induzione della memoria immunitaria innata negli invertebrati, inclusa la sovraregolazione o "allenamento" di percorsi regolatori come come Toll o Imd (Boutros et al,2002) e cambiamenti quantitativi e fenotipici nelle popolazioni di cellule immunitarie (Ro-drigues et al.,2010). Alcuni ricercatori hanno anche proposto la presenza di meccanismi di generazione della diversità negli insetti. Tali meccanismi candidati possono coinvolgere proteine correlate al fibrinogeno con alti tassi di diversificazione a livello genomico (Zhang et al.,2004) o sovraregolazione dell'espressione di recettori specifici come molecole di riconoscimento del peptidoglicano e lectine (Steiner, 2004).
In studi sperimentali sui topi sono stati riportati importanti indizi che l'immunità innata dei vertebrati ha anche caratteristiche adattive. Diversi studi di questo tipo hanno dimostrato che l'adescamento o l'addestramento dei topi con ligandi microbici può proteggere da infezioni letali. Ad esempio, l'immunità allenata indotta da -glucano (derivato da funghi) induce protezione contro l'infezione batterica da Staphylococcus aureus (Di Luzio e Williams, 1978; Marakalala et al, 2013). Allo stesso modo, il componente batterico del peptidoglicano muramil dipeptide induce protezione contro il Toxoplasma (Krahenbuhl et al, 1981) e la somministrazione di oligodeossinucleotide CpG protegge dalla sepsi e dalla meningite da Escherichia coli (Ribes et al, 2014). Inoltre, la flagellina dei batteri Gram-negativi può indurre protezione contro il batterio Gram-positivo Streptococcus pneumoniae (Munoz et al.,2010) e rotavirus (Zhang et al.,2014a). Oltre ai ligandi microbici, ci sono prove che alcune citochine pro-infiammatorie possono indurre un'immunità allenata: infezione di topi con una dose di IL ricombinante{10}} tre giorni prima dell'infezione da Pseudo-monas aeruginosa topi protetti contro la mortalità (van der Meer et al., 1988). Il carattere non specifico degli effetti immunitari allenati contrasta con un classico effetto memoria mediato dall'immunità adattativa e suggerisce l'attivazione di meccanismi immunitari innati non specifici. Un aspetto importante che dovrà essere studiato è la durata degli effetti protettivi dell'immunità allenata. Studi su topi e esseri umani hanno mostrato effetti dopo 3 mesi e anche un anno (Kleinnijenhuis et al, 2014), sebbene i dati epidemiologici basati sugli effetti protettivi eterologhi dei vaccini suggeriscano che saranno funzionali da almeno 3-a 5 anni.
L'immunità addestrata può mediare almeno alcuni degli effetti protettivi della vaccinazione. Prove convincenti provengono da studi che dimostrano che la vaccinazione con il bacillo del vaccino contro la tubercolosi Calmette Guerin (BCG), il vaccino più comunemente usato in tutto il mondo, induce una protezione indipendente dai linfociti T contro infezioni secondarie da Candida albicans, Schistosoma mansoni o influenza negli animali (Spencer et al. .,1977; Tribouley et al.1978; non può Wout et al.,1992). I dati sull'uomo completano questi studi: la vaccinazione BCG in volontari umani protegge da un'infezione sperimentale con il virus del vaccino contro la febbre gialla (Arts et al,2018), mentre ampi studi epidemiologici hanno riportato effetti protettivi eterologhi per la vaccinazione BCG e morbillo (Benn et al,2013 ; Goodridge et al, 2016). Inoltre, la latenza dell'herpesvirus aumenta la resistenza ai patogeni batterici Listeria monocytogenes e Yersinia pestis (Barton et al.,2007) con una protezione ottenuta attraverso una maggiore produzione di IFNy e l'attivazione sistemica dei macrofagi. Allo stesso modo, l'infezione con il parassita elmintico Nip-strongyles brasiliensis induce un fenotipo macrofagico a lungo termine che danneggia il parassita e induce protezione dalla reinfezione indipendentemente dai linfociti T e B (Chen et al.,2014).
Le principali popolazioni cellulari che sono state segnalate come responsabili della memoria immunitaria innata sono i monociti, i macrofagi derivati dai monociti e le cellule natural killer (NK). Mentre la protezione secondaria dall'infezione dipendente dai macrofagi non è specifica, la memoria immunitaria mediata dalle cellule NK può fornire una maggiore specificità. La prima prova della memoria delle cellule NK viene dalle osservazioni di diversi topi carenti di cellule T e B (RAG knockout, SCID e nu/nu) che sono in grado di montare robuste risposte di richiamo a sensibilizzatori di contatto a base di aptene (O'Leary et al, 2006). Le cellule NK possono mediare il contatto specifico dell'apteneipersensibilità(CHS) in questi animali, tuttavia la memoria delle cellule NK è limitata alle cellule residenti nel fegato di NK.1.1 più DX5-CXCR6 più CD49a più fenotipo (OLeary et al,2006; Paust et al,2010; Peng et al., 2013). Le cellule NK residenti nel fegato di topo possono sviluppare una memoria specifica verso una varietà di apteni e altri antigeni, comprese le particelle simili a virus (VLP); tuttavia, il meccanismo di riconoscimento dell'antigene non è noto (Paust et al.,2010). Nei macachi rhesus sono state osservate anche risposte delle cellule della memoria NK antigene-specifiche e di lunga durata (spleniche ed epatiche), suggerendo che le cellule NK della memoria antigene-specifiche possono esistere anche nell'uomo (Reeves et al., 2015)
Le cellule NK possono essere attivate dal citomegalovirus: dopo l'infezione con il citomegalovirus murino (mCMV)(Nabekura et al,2015; Schlums et al.,2015; Sun et al,2009; Sunset al.,2012), le cellule NK recanti il recettore Ly49H proliferano , persistente negli organi linfoidi e non linfoidi durante la fase di contrazione della risposta delle cellule NK. Dopo la reinfezione, le cellule NK "di memoria" subiscono un'espansione secondaria, degranulando rapidamente e rilasciando citochine, inducendo così una risposta immunitaria protettiva (Sun et al, 2009). Sono stati proposti numerosi meccanismi possibili per spiegare le proprietà di memoria delle cellule NK, che coinvolgono l'asse IL-12/IFNy (Sun et al,2012) o l'attivazione della molecola co-stimolante DNAM{{10 }} (molecola accessoria DNAX-1, CD226) (Nabekura et al.,2014).

La memoria NK indotta da CMV sembra essere specifica: studi sui topi non hanno dimostrato una maggiore reattività delle cellule di memoria NK indotte da mCMV contro altre infezioni come l'influenza o Listeria (Min-Oo e Lanier, 2014). Allo stesso modo, gli studi sull'uomo non mostrano alcuna reattività di NKG2C più CD57 più la popolazione di cellule NK espansa nell'(H) CMV umano più individui (Hendricks et al, 2014). È stato suggerito che anche le cellule NK innescate da citochine sviluppino proprietà simili alla memoria. Le cellule NK di topo e umane stimolate con una combinazione di IL12, IL15 e IL18 hanno mostrato una maggiore produzione di IFNy in risposta alla stimolazione secondaria con citochine o cellule tumorali settimane dopo l'innesco delle citochine (Cooper et al.,2009; Keppel et al,2013 ; Romee et al.,2012).
Le cellule linfoidi innate gruppo 2 (ILC2) che condividono il comune progenitore linfoide con le cellule NK, B e T, non possiedono recettori per l'antigene ma possono essere attivate dalle citochine. Mostrano anche il potenziale per "ricordare" il loro stato di attivazione e generare risposte potenziate alla stimolazione secondaria. Nel polmone, gli allergeni inalati stimolano le ILC2 a produrre IL-5 e IL-13 in modo IL{5}}dipendente (Halim et al.,2014). Dopo l'attivazione indotta da allergeni, le ILC2 polmonari subiscono un'espansione seguita da una fase di contrazione in cui non producono citochine. Una popolazione di ILC2 con esperienza di allergeni persiste nel polmone e nei linfonodi. In una sfida secondaria con allergeni non correlati, gli ILC2 simili alla memoria montano una risposta immunitaria più robusta. La sensibilizzazione dei topi con IL-33 è stata sufficiente per generare ILC2 di memoria che rispondono alla stimolazione secondaria dell'allergene indicando il carattere non specifico dell'antigene della memoria di ILC2 (Martinez-Gonzalez et al.,2016).
Queste osservazioni possono anche evidenziare il posizionamento unico di ILC e cellule NK all'incrocio evolutivo tra immunità innata e adattativa.
Presi insieme, questi studi complementari murini e umani dimostrano che le risposte immunitarie innate hanno la capacità di essere "allenate" e quindi esercitare un nuovo tipo di memoria immunologica in caso di reinfezione, per la quale è stato proposto il termine immunità allenata (Netea et al, 2016; Netea et al., 2011). Un'estensione del concetto di immunità addestrata è stata recentemente proposta per contenere anche tipi di cellule non immuni, come le cellule epiteliali (Cassone, 2018).
