Parte seconda MRI pesata in diffusione nel sistema genito-urinario
Jul 05, 2023
Imaging della prostata pesato in diffusione
DWI ha rappresentato una svolta nell'imaging oncologico, incluso l'imaging della prostata [43,44]. Ora costituisce la pietra angolare dell'imaging del cancro alla prostata che viene realizzato mediante risonanza magnetica multiparametrica (mpMRI) [45]. La prospettiva "multiparametrica" corrisponde a tre sequenze acquisite in un'unica sessione di risonanza magnetica. In primo luogo include la sequenza anatomica T2W raffigurante l'architettura zonale prostatica in almeno due diversi piani, principalmente nei piani assiale e in secondo luogo nei piani sagittale e/o coronale utilizzando immagini ad alta risoluzione. Quindi, vengono acquisite due sequenze funzionali nel piano assiale. La sequenza DW considerata viene eseguita prima della somministrazione del contrasto e seguita dall'imaging DCE, che a volte viene definito imaging della perfusione. Va notato che quest'ultimo richiede l'iniezione endovenosa di contrasto di gadolinio ad una portata elevata. Quando non viene eseguita l'imaging dinamico con mezzo di contrasto, la coppia di sequenze T2W e DW viene definita MRI biparametrica (bpMRI). La BpMRI corrisponde allo standard minimo di un esame contributivo senza perdita di performance diagnostica, come illustrato in uno studio condotto su 431 pazienti [46].
La maggior parte degli esami mpMRI della prostata si basano su mappe ADC fornite solo da due diversi valori b e un modello monoesponenziale in cui la diffusione tissutale è presumibilmente libera con distanze gaussiane distribuite [47]. Tuttavia, sono stati sviluppati modelli di diffusione più complessi per esplorare le proprietà dei tessuti microarchitettonici [48]. L'aumento del numero di numeri di coefficiente nei modelli matematici migliora la descrizione della diffusione dell'acqua nella prostata, come dimostrato da metodi statistici, come l'Akaike Information Criterion [47,49,50]. Ad esempio, l'aggiunta di un secondo parametro nel modello biesponenziale illustra meglio la differenza nelle proprietà di diffusione dovute a più compartimenti tissutali. Il contributo dei modelli multiesponenziale è stato studiato nello studio di Bourne et al. utilizzando il microimaging RM su campioni prostatici fissati in formalina [49]. Il comportamento del segnale voxel segue prima un rapido decadimento esponenziale e poi, da valori b superiori a 200 s/mm2, un lento decadimento esponenziale. Tali osservazioni hanno portato al modello biesponenziale "a tre coefficienti", chiamato modello di movimento incoerente intravoxel (IVIM), che tiene conto del flusso sanguigno nella rete capillare [51]. Il modello IVIM richiede molti valori b per produrre tre mappe parametriche rispettivamente della frazione di perfusione, della diffusione pura e del coefficiente di pseudo diffusione [47]. La pseudodiffusione ha origine dalla circolazione microscopica nel tessuto predominante a bassi valori b (<200 s/mm2 ) and can be differentiated from the pure diffusion prevailing at higher b-values secondary to Brownian motion within the extravascular space [51]. Furthermore, the diffusion in prostatic tissue at b-values higher than 1000 s/mm2 is influenced by the spatial partitioning by cellular membranes which separate extracellular and intracellular spaces. This leads to another representation of a bi-exponential model with specific coefficients named ADCslow and ADChigh introduced for prostate DW imaging by Mulkern [52]. While multiexponential models add new terms for the DW signal decay, other models of higher complexity were studied in prostate MR imaging, such as the stretched exponential model or diffusion kurtosis imaging (DKI), which are not currently used in the clinical routine [53].

Clicca qui per sapere cosa sono le Cistanche benefici
Fino ad oggi, il modello monoesponenziale mantiene la posizione elevata nella mpMRI della prostata eseguita di routine, grazie alla sua rapida elaborazione e interpretazione basata sulla mappa ADC. Tale modello non parametrico è ben integrato come standard clinico di routine [47]. Inoltre, la sua performance diagnostica è stata considerata superiore al modello IVIM [48,54]. In uno studio recente, il modello DKI non è risultato superiore al modello monoesponenziale per la rilevazione di tumori clinicamente significativi [55]. Tuttavia, come suggerito nelle linee guida PI-RADS (prostate imaging-reporting and data system), è essenziale interpretare la mappa ADC insieme alle immagini DW native [45]. La Figura 6 illustra un nodulo neoplastico che sorge nella zona periferica della prostata, che appare con valori ADC inferiori in combinazione con un focus iperintenso su immagini con valori b elevati. Tali risultati sono tipici della ridotta diffusione all'interno di un'area tumorale come conseguenza dell'elevata cellularità. È stato dimostrato che la densità cellulare misurata quantitativamente mediante tecniche istologiche è negativamente correlata ai valori di ADC [56,57]. Studi basati sul confronto tra immagini DW assiali e vetrini istologici hanno riportato una correlazione negativa tra i valori di ADC e il grado di differenziazione del tessuto tumorale, il punteggio di Gleason [58], che è più evidente nella zona periferica che nella zona di transizione. 59].
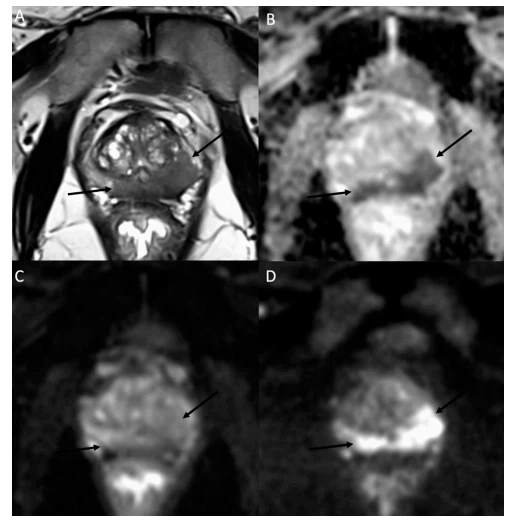
Figura 6. Immagini RM di una risonanza magnetica della prostata a 3T in un uomo di 78-anni con un PSA di 7,7 ng/mL. (A) L'immagine morfologica assiale T2W mostra un'area ipointensa (frecce) che si espande nella zona periferica del parenchima prostatico su entrambi i lati con un'infiltrazione tissutale predominante sul lato sinistro (B) La corrispondente mappa ADC ottenuta adattando un modello monoesponenziale utilizzando le immagini b-50 (C) e b-1500 (D). Come tipico esempio di adenocarcinoma prostatico di alto grado, le immagini b-50 (C) tob-1500 (D) mostrano un segnale in aumento nel tessuto neoplastico a causa delle proprietà di restrizione della diffusione nel Gleason istologicamente provato 9 carcinoma della prostata. Questi risultati MR sono stati riportati come aspiranti 5.
Il ruolo essenziale della tecnica di diffusione nell'imaging della prostata è ben illustrato dal punteggio PI-RADS. Questo sistema di punteggio è stato stabilito da una rappresentanza congiunta dell'American College of Radiology (ACR), della European Society of Urogenital Radiology (ESUR) e della AdMeTech Foundation. Il punteggio PI-RADS varia da 1 a 5, con reperti RM normali (1) a reperti RM altamente sospetti di neoplasia prostatica maligna (5). La versione 1.0 è stata pubblicata nel 2{{10}}12, seguita dalla versione 2.{{20}} nel 2014 e la versione 2.1 nel 2019 [60–62]. Nelle versioni da 1.0 a 2.0, importanti modifiche hanno rivelato il ruolo dell'imaging di diffusione nel rilevamento del cancro alla prostata. Nella versione 1.0, tutte le sequenze eseguite nella risonanza magnetica della prostata (T2W, DWI e DCE) sono state considerate uguali per il rilevamento del cancro. Dalla versione PI-RADS 2.0, DWI costituisce un fattore chiave di apprezzamento. Nella zona periferica della prostata, il punteggio PI-RADS del sospetto tumorale si basa principalmente sui risultati della diffusione come illustrato nella Figura 6. Nella zona di transizione, il parenchima può essere modificato dall'iperplasia stromale e ghiandolare, risultando in un complesso e caotico tessuto che richiede le informazioni anatomiche fornite dalle sequenze T2W. Tuttavia, DWI è essenziale per completare l'analisi, consentendo l'aggiornamento di "aree equivoche" a lesioni con punteggio PI-RADS più elevato. In uno studio recente, le prestazioni del punteggio PI-RADS nel rilevamento del cancro alla prostata sono state caratterizzate da un elevato valore predittivo negativo (NPV) del 94,1% per un cut-off PI-RADS a 3 e un VAN dell'85,5% con un cut-off a 4 [63]. L'esame RM della prostata fornisce uno strumento prezioso per la stratificazione del rischio di cancro. Tuttavia, una meta-analisi ha rilevato che il VAN della mpMRI varia dal 63% al 98%, il che illustra i rimanenti limiti alla rilevazione di lesioni significative del cancro alla prostata in alcuni pazienti [64,65]. La nuova versione 2.1 del punteggio PI-RADS considera il DWI come riferimento per il rilevamento di tumori prostatici significativi nella zona periferica e come strumento di supporto di grande valore per la zona di transizione accanto alla sequenza T2W dominante.

Estratto di cistanche
Nel sistema di punteggio PI-PRADS, la valutazione del punteggio è comunemente basata sull'interpretazione qualitativa e visiva dell'mpMRl. In tale cornice, l'esperienza del radiologo e la riproducibilità del punteggio devono essere chiarite. In uno studio di 2017 di Kwon et al., gli autori riportano un eccellente accordo interosservatore (k > 0.870) nel punteggio DWI e un accordo da buono a eccellente ( k > 0,771) nel punteggio PI-RADS finale utilizzando PI-RADS v2.0 tra due radiologi di 11 anni e 1- anni di esperienza, rispettivamente (66). Tuttavia, studi precedenti hanno riportato punteggi di concordanza interosservatore inferiori ({{13 }}). Pertanto, per limitare la variabilità nell'interpretazione della mpMRI, l'ottimizzazione del protocollo RM è il primo e necessario passo. inclusa la valutazione del DWI vulnerabile agli artefatti dall'aria rettale.Inoltre, la curva di apprendimento e la durata della formazione del radiologo hanno un effetto di miglioramento sull'accordo inter-lettore (70,71).The European Society of Urogenital Radiology (ESUR) e il consenso della sezione di imaging urologico (ESU) dell'Associazione europea di urologia (EAU) ha offerto alcune raccomandazioni suggerendo che i radiologi dovrebbero essere addestrati con una soglia di casi supervisionati prima della segnalazione indipendente, nonché una soglia minima annuale di letture [70]. Il gruppo di esperti e gli studi suggeriscono un minimo di 100 casi di formazione prima di ottenere un AUC alla pari con lettori più esperti [70,71]. Tuttavia, i requisiti di formazione possono essere drasticamente modificati dall'introduzione di nuovi algoritmi di apprendimento automatico per assistere l'analisi MRI della prostata [72,73].
Incorporando le sequenze DWI nella mpMRI della prostata, la tecnica si è evoluta fino a raggiungere un ruolo dominante in ambito clinico. Fino a questo punto, l'imaging clinico RM della prostata era limitato alla stadiazione locale prima del campionamento bioptico casuale mediante ecografia transrettale. La risonanza magnetica ora detiene più compiti nella gestione del cancro alla prostata, compreso il rilevamento del cancro alla prostata prima delle biopsie, la stadiazione preoperatoria, la sorveglianza attiva del cancro di basso grado comprovato dalla biopsia e il rilevamento della recidiva locale dopo la prostatectomia radicale o altri schemi di terapia locale. Siddqui et al. dimostrato l'importanza di un esame MRI della prostata prima delle biopsie prostatiche per migliorare il rilevamento di lesioni tumorali di alto grado. In effetti, la biopsia mirata basata su immagini RM coregistrate con immagini ecografiche durante la procedura ha portato al 30 percento in più di rilevamento del cancro ad alto rischio rispetto alla procedura standard [74]. Questa scoperta si traduce nel 20-30 percento delle lesioni significative del cancro alla prostata che non vengono rilevate dalle biopsie transrettali sistematiche standard [75,76]. Inoltre, il ruolo della risonanza magnetica della prostata nella stadiazione locale è stato recentemente valutato da Caglic et al. [77]. Secondo loro, la mpMRI produce sensibilità e specificità del 66,2% e dell'84,6% nell'estensione extracapsulare e dell'83,3% e del 97,8% nell'invasione delle vescicole seminali, con risultati comparabili utilizzando l'esame RM parametrico. Da questo aspetto, la mpMRI fornisce informazioni locali vitali consentendo all'urologo di apprezzare la tattica chirurgica per preservare i fasci neurovascolari nella prostatectomia radicale assistita da robot Da-Vinci. Dopo la chirurgia radicale, la mpMRI può essere utilizzata per analizzare la situazione dell'operazione in caso di recidiva biochimica. Tuttavia, l'esecuzione dell'esame dipende dai livelli di antigene prostatico specifico (PSA) e dal grado di Gleason della neoplasia iniziale, secondo lo studio di Venkatesan et al. che ha riportato l'87,2% di esami negativi nei casi di PSA inferiore a 0,5 ng/ml nei tumori di grado inferiore e l'88,9% di esami positivi nei casi di PSA superiore a 1,5 ng/ml nei tumori di grado superiore [78]. Da questa osservazione, il contributo diagnostico della mpMRI è più rilevante nelle combinazioni intermedie di livelli di PSA e tumori di grado Gleason.
In conclusione, DWI rappresenta un importante progresso nel rilevamento del cancro alla prostata mediante risonanza magnetica. La risonanza magnetica è riconosciuta come un fattore chiave nell'attuale sistema di punteggio PI-RADS 2.1, aggiornato l'ultima volta nel 2019. La mappa ADC quantitativa derivata dall'acquisizione di immagini dei valori b adattando il modello monoesponenziale viene utilizzata di routine in ambito clinico e consente di ottenere una caratterizzazione tissutale rappresentativa. Bassi valori di ADC sono correlati con tessuti tumorali ad alto punteggio di Gleason composti da forti aree cellulari. In futuro, il ruolo di DWI nella risonanza magnetica biparametrica che combina immagini T2W e DW senza somministrazione di contrasto deve essere definito più chiaramente come un potenziale metodo per una migliore stratificazione del rischio di cancro e per guidare le biopsie mirate alla prostata.

Capsule di cistanche
Imaging della vescica pesato in diffusione
La risonanza magnetica della vescica nella malattia neoplastica sta emergendo mentre la stadiazione locale del carcinoma uroteliale si basa essenzialmente sui reperti cistoscopici e sull'analisi istologica della resezione transuretrale del tumore. Il criterio principale per la decisione terapeutica è l'integrità o l'invasione dello strato muscolare detrusoriale, indirizzando il trattamento verso la chirurgia radicale o la resezione locale endoscopica più conservativa. Questa dualità porta alla distinzione principale tra carcinoma muscolare superficiale non invasivo e tumore muscolo-invasivo. Un punteggio, il Vesical Imaging Reporting And Data System (VI-RADS) è stato introdotto nel 2018 [79] in aggiunta ai gradi su una scala da 1 a 5. Mentre il punteggio PI-RADS nel cancro alla prostata mpMRI è dedicato alla probabilità di cancro significativo, il punteggio VI-RADS nel cancro della vescica classifica la stadiazione locale della lesione tumorale nella profondità della parete della vescica. Ogni sequenza della mpMRI viene valutata per la presenza di una discontinuità nello strato muscolare normale della vescica, contribuendo ad assegnare una probabilità di invasione muscolare compresa tra 1 (invasione muscolare improbabile) e 5 (invasione muscolare molto probabile). Le immagini T2W forniscono una prima valutazione a causa della loro rappresentazione anatomica superiore degli strati della vescica prima che l'imaging DWI e DCE contribuisca alla categoria finale VI-RADS [79,80]. Le prestazioni del sistema di punteggio sono state esaminate da Jury et al. [80] sulla base di sei relazioni precedenti. Impostando un cut-off a VI-RADS 4, un intervallo di sensibilità e specificità tra il 76-91 percento e il 76-93 percento, rispettivamente, con un punteggio di concordanza interosservatore superiore a 0,7 [80]. È chiaro che la DWI è una parte essenziale della mpMRI nella stadiazione del cancro della vescica e ulteriori convalide cliniche del punteggio VI-RADS potrebbero richiedere un contributo crescente della tecnica nella pratica di routine.
Imaging del pene pesato in diffusione
Nella pratica corrente, la risonanza magnetica del pene è più frequentemente richiesta dagli urologi per la stadiazione locale di tumori che crescono principalmente nel glande o nel prepuzio, per la frattura del pene e la malattia di Peyronie. Le immagini T2W ad alta risoluzione consentono una rappresentazione precisa dell'estensione tumorale all'interno dei corpi cavernosi o della parete uretrale, nonché delle lacrime traumatiche o dell'ispessimento infiammatorio nella tunica albuginea dei corpi cavernosi. In condizioni cliniche così ben definite, DWI ha un ruolo meno preponderante. Tuttavia, i tumori maligni primari, più comunemente i carcinomi a cellule squamose, possono essere ben identificati utilizzando le mappe DWI e ADC. L'infiltrazione neoplastica del pene mostra valori di ADC inferiori, inversamente proporzionali al grado istologico del tumore, secondo lo studio di Barua et al. in 26 pazienti [81]. Nei casi di fimosi grave, i tumori potrebbero essere oscurati [82] dalla cute di copertura, rendendo l'esame RM particolarmente appropriato per un'esplorazione locale alla ricerca di tessuto neoplastico prima dell'intervento chirurgico.
Imaging testicolare pesato in diffusione
Come per altri organi, DWI è integrato nei protocolli MRI standard per caratterizzare le masse intratesticolari, contribuendo a un protocollo multiparametrico scrotale simile all'imaging della prostata. Gli studi hanno studiato il ruolo del DWI nella differenziazione tra tumori a cellule non germinali derivanti nel tessuto testicolare interstiziale da neoplasie a cellule germinali o tra tumori seminomatosi o non seminomatosi [83,84]. In effetti, DWI fornisce informazioni funzionali sull'architettura istologica microstrutturale che può combinarsi con le proprietà del tessuto microvascolare portate dall'imaging DCE per definire la diagnosi. Tuttavia, la risonanza magnetica contribuisce solo in alcuni casi specifici a causa dell'elevata capacità degli ultrasuoni di dimostrare tumori maligni come masse vascolarizzate e solide [85]. La risonanza magnetica può essere eseguita quando i reperti ecografici non sono conclusivi in lesioni simili a masse, come ematoma, infarto segmentale o infiammazione o infezione granulomatosa [85,86]. Con il supporto della Società Europea di Radiologia Urogenitale (ESUR), le raccomandazioni sono redatte dallo Scrotal and Penile Imaging Working Group sulle indicazioni appropriate della mpMRI scrotale [87]. Da una prospettiva promettente, gli studi hanno dimostrato un legame tra l'ADC e la funzione spermatogenica del testicolo [88], sebbene non sia ancora seguita alcuna convalida clinica. È interessante notare che uno studio di Ntorkou et al. su 49 uomini hanno discusso la potenziale capacità dell'ADC di prevedere un'estrazione di spermatozoi testicolare con microdissezione riuscita per il recupero dello sperma in pazienti che presentano azoospermia non ostruttiva [89].

Supplemento cistanche
Imaging renale pesato in diffusione
DWI non ha attualmente alcuna indicazione stabilita nella diagnosi clinica e nella gestione della malattia renale. Tuttavia, numerosi studi hanno riportato osservazioni promettenti a sostegno del possibile ruolo del DWI in varie malattie renali. La descrizione tecnica dei diversi metodi di acquisizione o analisi specifici del DWI renale va oltre lo scopo di questa rassegna e può essere ottenuta altrove [90,91].
In oncologia, l'ADC non è in grado di distinguere in modo robusto tra tumori renali maligni e benigni, ma può essere utile per caratterizzare i sottotipi tumorali [92]. In una meta-analisi di 1126 lesioni renali da 13 studi, i carcinomi a cellule renali (RCC) a cellule chiare hanno dimostrato valori di ADC più elevati rispetto a RCC a cellule non chiare, angiomiolipomi a basso contenuto di grassi, RCC papillari e RCC cromofobi, ma valori di ADC inferiori rispetto oncocitomi [93]. Sebbene questi risultati siano stati recentemente confermati utilizzando l'ADC [92] o l'imaging RM del tensore della curtosi, un tipo più avanzato di analisi DWI [94], la moderata sensibilità e specificità riportate da questi lavori potrebbero non essere sufficienti affinché DWI sia un singolo test affidabile per differenziare i sottotipi di RCC [93]. In uno studio su 46 pazienti con malattia di Von Hippel-Lindau (VHL), l'ADC al basale era correlato negativamente con il tempo di raddoppio del volume di 100 RCC a cellule chiare [95]. Poiché la sorveglianza attiva e la chirurgia con risparmio renale sono componenti importanti della gestione dei pazienti con VHL, la valutazione della crescita tumorale mediante ADC potrebbe essere un importante sviluppo del DWI in futuro [96].
La pielonefrite acuta (APN) può essere diagnosticata mediante DWI con una riduzione del valore di ADC nell'area di infiltrazione delle cellule infiammatorie [97-99]. I fuochi pielonefritici appaiono scuri sulla mappa ADC. Le prestazioni del DWI per rilevare l'APN sono simili sia alla TC con mezzo di contrasto (CECT) [100] che alla scintigrafia renale [101-103] e probabilmente migliori dell'imaging nucleare per il rilevamento di focolai infiammatori multipli [103]. Ciò potrebbe essere vantaggioso in situazioni ambigue in cui la diagnosi di APN è incerta, specialmente nei reni trapiantati e nei bambini. Pertanto, DWI potrebbe sostituire gli strumenti diagnostici tradizionali senza la necessità di mezzi di contrasto allo iodio e risparmiando dosi di radiazioni. Come sottolineato da un recente rapporto di una task force di imaging della Società Europea di Radiologia Pediatrica [104], il DWI non fa attualmente parte delle attuali linee guida cliniche e sono necessari ulteriori studi per definire meglio il ruolo clinico del DWI nel caso di APN.
Nella disfunzione acuta del trapianto, i valori di ADC sono ridotti in caso di rigetto acuto (AR), necrosi tubulare acuta (ATN) o tossicità immunosoppressiva, ma DWI non è in grado di distinguere tra queste patologie [98,105-110]. Un'interessante applicazione del DWI può essere la selezione di pazienti con disfunzione acuta del trapianto che possono beneficiare di una biopsia renale. In uno studio retrospettivo su 40 reni trapiantati, una combinazione di parametri DW-MRI qualitativi e quantitativi ha predetto la gravità dei risultati istopatologici rispetto ai cambiamenti normali o lievi [111]. Questi risultati sono stati confermati in uno studio prospettico su 33 pazienti trapiantati che necessitavano di un intervento [112]. DWI ha aiutato a differenziare i pazienti con o senza la necessità di cambiamenti nella gestione clinica a seguito di una biopsia renale e può essere un passo importante in un cambio di paradigma verso la biopsia virtuale [113].
Sia i valori di ADC corticale che midollare dei reni diabetici sono ridotti rispetto ai valori di ADC dei reni ben funzionanti [114-116] e sono correlati agli stadi clinici della nefropatia diabetica [117]. Tuttavia, l'utilità clinica di DWI per i pazienti diabetici non è ancora dimostrata e i risultati di ampi studi clinici in corso, come i biomarcatori di imaging prognostico per la malattia renale diabetica (iBEAt) (Identificatore ClinicalTrials.gov: NCT03716401) aiuteranno in questa materia.
Una delle applicazioni più promettenti del DWI è la stima della fibrosi renale nei pazienti con malattia renale cronica (CKD), che è un marker prognostico chiave per la diminuzione della funzione renale e la progressione della CKD. Questa affermazione ha due argomenti principali. In primo luogo, i valori di ADC sono correlati alla funzione renale [118-123] e il DWI è una tecnica di imaging non invasiva accurata per la diagnosi precoce e la stadiazione della malattia renale cronica, come mostrato da una meta-analisi [124]. In secondo luogo, numerosi studi clinici hanno dimostrato direttamente che i valori di ADC corticale e altri parametri correlati alla diffusione sono linearmente correlati alla fibrosi renale nei pazienti con CKD, come valutato dalla biopsia renale [105,125-133]. Con l'aumentare della fibrosi, i valori di ADC corticale diminuiscono molto più dei valori di ADC midollare, determinando un'inversione della differenza cortico-midollare di ADC o il cosiddetto ∆ADC che può essere osservato nelle immagini [129] (vedere Figura 7) . DWI può anche distinguere tra i diversi livelli di fibrosi [127,128].
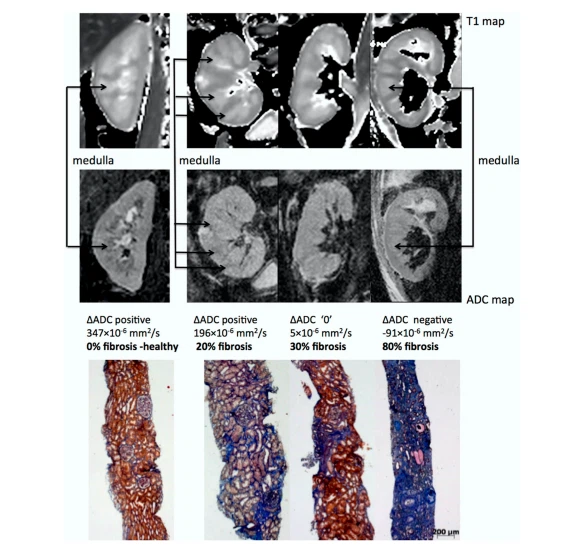
Figura 7. Biopsia rappresentativa e immagini RM in pazienti con malattia renale cronica. Le mappe morfologiche MOLLI TI sono state utilizzate per il posizionamento delle regioni di interesse (riga superiore) e delle mappe ADC (riga inferiore) per tre pazienti che mostravano diversi casi di AADC: positivo, zero e negativo; insieme ai corrispondenti livelli di fibrosi dall'istologia (colorazione tricromica di Masson). L'inversione della differenza ADC corticomidollare incontra il grado crescente di fibrosi renale. Adattato dalla Figura 7 di Rif. [129] con permesso. Copyright 2016 Springer Natura.
L'esatta spiegazione fisiologica e meccanicistica del legame tra i valori di DWI e la fibrosi renale non è completamente compresa, ma potrebbe essere il risultato di due principali eventi sinergici che si verificano nello sviluppo della fibrosi renale nella CKD: (1) un aumento della densità cellulare e l'extra -matrice cellulare che riduce il libero movimento dell'acqua e (2) una riduzione della perfusione microvascolare e della mobilità dell'acqua indotta dalla filtrazione prevista con compromissione
funzione renale(134). È interessante notare che la correlazione della DWI con la fibrosi renale è indipendente dalla funzione renale misurata dall'eGFR, supportando ulteriormente il ruolo della DWI come surrogato della fibrosi renale (127). Se la DWI può consentire di ridurre il numero di le biopsie renali predittive della quantità di fibrosi interstiziale nella CKD non sono attualmente note e necessitano di ulteriori valutazioni.
Un'altra potenziale applicazione del DWI nella CKD è correlata alla previsione della sua evoluzione. Recentemente, tre gruppi di ricerca indipendenti hanno osservato che il DWI al basale era correlato al declino della funzione renale (126,135,136).In uno studio con 197 pazienti con CKD, la previsione del peggior esito renale, come mostrato nella Figura 8, era indipendente dall'età al basale, dal sesso, dall'eGFR, e proteinuria, suggerendo fortemente che DWl potrebbe essere un marcatore prognostico indipendente di CKD.

Figura 8. Curve di sopravvivenza di Kaplan-Meier, stratificate in base alla differenza corticomidollare del coefficiente di diffusione apparente AADC nei pazienti con malattia renale cronica. L'outcome primario era un calo dell'eGFR > 30% o terapia renale sostitutiva. Un AADC negativo è stato associato a un rapido declino della funzione renale. Cl, intervallo di confidenza; HR, rapporto di rischio. Adattato dalla Figura 2 del Rif.[126] con permesso. Copyright 2016 Springer Natura.
In conclusione, DWI mostra una forte promessa di caratterizzare i tumori renali, rilevare APN e quantificare la fibrosi renale nei pazienti diabetici e CKD. Con gli studi clinici in corso e gli sforzi internazionali per l'uniformizzazione metodologica (137), è probabile che il suo potere diagnostico e predittivo sia notevolmente migliorato.L'uso di DWI può essere ulteriormente amplificato dallo sviluppo della risonanza magnetica multiparametrica che consente una valutazione aggiuntiva simultanea del sangue renale flusso e ossigenazione così come altri parametri morfometrici come il tempo di rilassamento Tl sopra DWI (128).
Limiti dello studio
Questa recensione si basa su un'analisi della letteratura eseguita utilizzando il database PubMed. Per ogni organo genito-urinario, gli studi più rilevanti sono in termini di recency e rappresentazione. è stato selezionato l'impatto nativo nel campo del DWI. Le query sono state eseguite cercando nel database le parole chiave riguardanti l'organo coinvolto e coinvolgendo l'imaging di diffusione e/o la risonanza magnetica. Tuttavia, questo lavoro non riporta studi nel modo in cui fa una meta-analisi strutturata includendo articoli scientifici che soddisfano criteri sistematici. La pertinenza delle opere selezionate è stata stabilita dal punto di vista della nostra pratica attuale e dagli esami RM regolarmente eseguiti presso la nostra istituzione. In tale contesto, la selezione dello studio contiene una parte riconosciuta della soggettività che si basa principalmente sull'esperienza combinata degli autori.

Cistanche tubulosa
Conclusioni
DWI è già una tecnica di imaging consolidata per la valutazione del sistema genito-urinario con il potenziale per un miglioramento significativo. Nel carcinoma pelvico femminile e nel carcinoma prostatico, il DWI fa parte delle linee guida internazionali per la diagnosi, la stadiazione e la valutazione delle recidive. DWI è anche un fattore determinante nei punteggi di rischio standardizzati O-RADS e PI-RADS. Nel rene, le applicazioni più promettenti del DWI possono essere la quantificazione della fibrosi renale e la previsione dell'evoluzione della malattia nella malattia renale cronica. Per integrare ulteriormente il DWI nelle strategie di diagnosi e nella gestione del paziente, la prossima sfida sarà la standardizzazione dei protocolli di acquisizione e analisi.
Riferimenti
43. Blackledge, MD; Leach, M.; Collins, D.; Koh, D.-M. L'imaging RM computerizzato pesato in diffusione può migliorare il rilevamento del tumore. Radiologia 2011, 261, 573–581. [CrossRef] [PubMed]
44. Lim, Hong Kong; Kim, JK; Kim, KA; Cho, K.-S. Cancro alla prostata: mappa del coefficiente di diffusione apparente con immagini ponderate T2- per il rilevamento: uno studio multilettore. Radiologia 2009, 250, 145–151. [CrossRef] [PubMed]
45. Collegio americano di radiologia. PIRADS Imaging della prostata—Reporting and Data System v2.1. 2019. Disponibile online: https: //www.acr.org/-/media/ACR/Files/RADS/Pi-RADS/PIRADS-V2-1.pdf (accesso il 1° febbraio 2021).
46. Pesapane, F.; Acquasanta, M.; Di Meo, R.; Agazzi, GM; Tantrige, P.; Coderi, M.; Schiaffino, S.; Rotella, F.; Esseridou, A.; Sardanelli, F. Confronto di sensibilità e specificità della risonanza magnetica prostatica biparametrica rispetto a quella multiparametrica nella rilevazione del cancro alla prostata in 431 uomini con livelli elevati di antigene prostatico specifico. Diagnostica 2021, 11, 1223. [CrossRef] [PubMed]
47. Wichtmann, BD; Zollner, FG; Attenberger, UI; Schönberg, SO Multiparametric MRI nella diagnosi del cancro alla prostata: fondamenti fisici, limitazioni e progressi prospettici della risonanza magnetica pesata in diffusione. RöFo-Fortschr. Geb. Röntgenstrahlen Bildgeb. Verfahr. 2021, 193, 399–409. [CrossRef]
48. Quentin, M.; Blondin, D.; Klasen, J.; Lanzmann, RS; Miese, F.‑R.; Arsov, C.; Albers, P.; Antoch, G.; Wittsack, H.‑J. Confronto di diversi modelli matematici di RM della prostata pesata in diffusione. Magn. Risonanza. Imaging 2012, 30, 1468–1474. [CrossRef]
49. Bourne, RM; Panagiotaki, E.; Bonger, A.; Sved, P.; Watson, G.; Alexander, DC Classifica teorica dell'informazione di quattro modelli di attenuazione della diffusione nel tessuto prostatico fresco e fisso ex vivo. Magn. Risonanza. Med. 2013, 72, 1418–1426. [CrossRef]
50. Liang S.; Panagiotaki, E.; Bonger, A.; Nave.; Sved, P.; Watson, G.; Bourne, R. Classifica basata sulle informazioni di 10 modelli compartimentali di attenuazione del segnale ponderata in diffusione nel tessuto prostatico fisso. NMR Biomedico. 2016, 29, 660–671. [CrossRef]
51. Le Bihan, D.; Bretone, E.; Lallemand, D.; Aubin, ML; Vignaud, J.; Laval-Jeantet, M. Separazione della diffusione e della perfusione nell'imaging RM con movimento incoerente intravoxel. Radiologia 1988, 168, 497–505. [CrossRef]
52. Mulkern, RV; Barnes, COME; Haker, SI; Appeso, YP; Rybicki, FJ; Maier, SE; Tempany, CM Caratterizzazione biesponenziale delle curve di decadimento della diffusione dell'acqua nel tessuto prostatico su un intervallo esteso di fattore b. Magn. Risonanza. Imaging 2006, 24, 563–568. [CrossRef]
53. Brancato, V.; Cavaliere, C.; Salvatore, M.; Monti, S. Modelli non gaussiani di imaging pesato in diffusione per il rilevamento e la caratterizzazione del cancro alla prostata: una revisione sistematica e una meta-analisi. Sci. Rep. 2019, 9, 16837. [CrossRef] [PubMed]
54. Dopfert, J.; Lemke, A.; Weidner, A.; Schad, LR Indagine sul cancro alla prostata mediante imaging del movimento incoerente intravoxel pesato in diffusione. Magn. Risonanza. Imaging 2011, 29, 1053–1058. [CrossRef] [PubMed]
55. Parco, H.; Kim, SH; Lee, Y.; Figlio, JH Confronto delle prestazioni diagnostiche tra i parametri di imaging della curtosi da diffusione e l'ADC monoesponenziale per la determinazione del cancro clinicamente significativo nei pazienti con carcinoma della prostata. Addome. Radiol. 2020, 45, 4235–4243. [CrossRef]
56. Gibbs, p.; Liney, GP; Sottaceti, MD; Zelhof, B.; Rodrigues, G.; Turnbull, Correlazione LW delle misurazioni di ADC e T2 con densità cellulare nel cancro alla prostata a 3.0 Tesla. Indagare. Radiol. 2009, 44, 572–576. [CrossRef] [PubMed]
57. Kwak, JT; Sankineni, S.; Xu, S.; Turkbey, B.; Choyke, Polonia; Pinto, Pennsylvania; Merino, MJ; Wood, BJ Correlazione della risonanza magnetica con l'istopatologia digitale nella prostata. Int. J. Calcola. Assistere. Radiol. Surg. 2016, 11, 657–666. [CrossRef] [PubMed]
58. Dhatt, R.; Choy, S.; Co, SJ; Ischia, J.; Kozlowski, P.; Harris, CA; Jones, EC; Nero, PC; Goldenberg, SL; Chang, SD MRI della prostata con e senza bobina endorettale a 3 T: correlazione con il punteggio di Gleason istopatologico a monte intero. Sono. J. Roentgenol. 2020, 215, 133–141. [CrossRef]
59. Surov, A.; Meyer, HJ; Wienke, A. Correlazioni tra coefficiente di diffusione apparente e punteggio di Gleason nel cancro alla prostata: una revisione sistematica. Euro. Urol. Oncol. 2020, 3, 489–497. [CrossRef]
60. Barentsz, JO; Richenberg, J.; Clementi, R.; Choyke, P.; Verma, S.; Villeirs, G.; Rouviere, O.; Logager, V.; Fütterer, JJ ESUR prostata RM linee guida 2012. Eur. Radiol. 2012, 22, 746–757. [CrossRef] [PubMed]
61. Turkbey, B.; Rosenkranz, AB; Haider, Massachusetts; Padhani, AR; Villeirs, G.; Macura, KJ; Tempany, CM; Choyke, Polonia; Cornud, F.; Margolis, DJ; et al. Reporting per imaging della prostata e sistema di dati versione 2.1: 2019 Aggiornamento del Reporting per imaging della prostata e sistema di dati versione 2. Eur. Urol. 2019, 76, 340–351. [CrossRef]
62. Weinreb, JC; Barentsz, JO; Choyke, Polonia; Cornud, F.; Haider, Massachusetts; Macura, KJ; Margolis, D.; Schnall, MD; Shtern, F.; Tempany, CM; et al. PI-RADS Prostate Imaging—Reporting and Data System: 2015, Versione 2. Eur. Urol. 2016, 69, 16–40. [CrossRef]
63. Tsai, WC; Campo, L.; Stewart, S.; Schultz, M. Revisione dell'accuratezza della prostata MRI multiparametrica nel rilevare il cancro alla prostata all'interno di un servizio di segnalazione locale. J. Med Imaging Radiat. Oncol. 2020, 64, 379–384. [CrossRef] [PubMed]
64. Felker, ER; Margolis, DJ; Nassiri, N.; Marks, LS Stratificazione del rischio di cancro alla prostata con risonanza magnetica. Urol. Oncol. Semin. Orig. Indagare. 2016, 34, 311–319. [CrossRef]
65. Futterer, JJ; Briganti, A.; De Visschere, P.; Emberton, M.; Giannarini, G.; Kirkham, A.; Taneja, SS; Thoeny, H.; Villeirs, G.; Villers, A. Il cancro alla prostata clinicamente significativo può essere rilevato con la risonanza magnetica multiparametrica? Una revisione sistematica della letteratura. Euro. Urol. 2015, 68, 1045–1053. [CrossRef] [PubMed]
66. Kwon, M.-R.; Kim, CK; Kim, J.‑H. PI-RADS versione 2: valutazione dell'interpretazione dell'imaging pesata in diffusione tra b=1000 e b=1500 s mm–2. Fr. J. Radiol. 2017, 90, 20170438. [CrossRef]
67. Rosenkranz, AB; Ginocchio, L.; Cornfeld, D.; Frömming, AT; Gupta, RT; Turkbey, B.; Vestfalen, AC; Babb, J.; Margolis, DJ Riproducibilità tra osservatori del lessico PI-RADS versione 2: uno studio multicentrico di sei radiologi esperti della prostata. Radiologia 2016, 280, 793–804. [CrossRef]
68. Müller, BG; Shih, JH; Sankineni, S.; Marco, J.; Rais-Bahrami, S.; Giorgio, AK; De La Rosetta, JJMCH; Merino, MJ; Legno, B.; Pinto, P.; et al. Cancro alla prostata: accordo e accuratezza tra osservatori con il sistema di segnalazione e dati di imaging della prostata rivisto all'imaging RM multiparametrico. Radiologia 2015, 277, 741–750. [CrossRef]
69 Giganti, F.; Kirkham, A.; Kasivisvanathan, V.; Papoutsaki, M.-V.; Punwani, S.; Emberton, M.; Moore, CM; Allen, C. Comprendere PI-QUAL per la qualità della risonanza magnetica della prostata: un pratico primer per i radiologi. Approfondimenti sull'imaging 2021, 12, 59. [CrossRef] [PubMed]
70 de Rooij, M.; Israele, B.; Tummers, M.; Ahmed, HU; Barrett, T.; Giganti, F.; Hamm, B.; Logager, V.; Padhani, A.; Panebianco, V.; et al. Dichiarazioni di consenso ESUR/ESUI sulla risonanza magnetica multiparametrica per il rilevamento del carcinoma prostatico clinicamente significativo: requisiti di qualità per l'acquisizione, l'interpretazione e la formazione delle immagini dei radiologi. Euro. Radiol. 2020, 30, 5404–5416. [CrossRef]
71. Gatti, M.; Faletti, R.; Calleris, G.; Giglio, J.; Berzovini, C.; Gentile, F.; Mara, G.; Misischi, F.; Molinaro, L.; Bergamasco, L.; et al. Rilevamento del cancro alla prostata con risonanza magnetica parametrica (bpMRI) da parte di lettori con diversa esperienza: prestazioni e confronto con multiparametrico (mpMRI). Addome. Radiol. 2019, 44, 1883–1893. [CrossRef]
72 Bertelli, E.; Mercatelli, L.; Marzi, C.; Pachetti, E.; Baccini, M.; Barucci, A.; Colantonio, S.; Gherardini, L.; Lattavo, L.; Pascali, MA; et al. Previsione automatica e deep learning dell'aggressività del cancro alla prostata utilizzando la risonanza magnetica multiparametrica. Davanti. Oncol. 2022, 11, 802964. [CrossRef]
73. Hosseinzadeh, M.; Saha, A.; Marca, P.; Slootweg, I.; de Rooij, M.; Huisman, H. Rilevazione del cancro alla prostata assistita dall'apprendimento profondo su risonanza magnetica biparametrica: requisiti minimi di dimensione dei dati di addestramento ed effetto della conoscenza precedente. Euro. Radiol. 2021, 32, 2224–2234. [CrossRef] [PubMed]
74. Siddiqui, M.; Rais-Bahrami, S.; Turkbey, B.; Giorgio, AK; Rothwax, J.; Shakir, N.; Okoro, C.; Raskol'nikov, D.; Parnes, HL; Linehan, WM; et al. Confronto tra biopsia guidata da fusione RM/ultrasuoni e biopsia guidata da ultrasuoni per la diagnosi del cancro alla prostata. JAMA J.Am. Associazione Med. 2015, 313, 390–397. [CrossRef] [PubMed]
75. Boesen, L. risonanza magnetica multiparametrica nel rilevamento e stadiazione del cancro alla prostata. Dan. Med. G. 2017, 64, 5327.
76. Serefoglu, CE; Altinova, S.; Ugras, NS; Akincioglu, E.; Asil, E.; Balbay, D. Quanto è affidabile una 12-procedura di biopsia prostatica di base per l'individuazione del cancro alla prostata? Potere. Urol. Assoc. J. 2013, 7, 293. [CrossRef]
77. Caglic, I.; Sushentsev, N.; Shah, N.; Warren, AY; Agnello, peso corporeo; Barrett, T. Confronto tra risonanza magnetica prostatica parametrica e multiparametrica per il rilevamento dell'estensione extracapsulare e dell'invasione delle vescicole seminali in pazienti naïve alla biopsia. Euro. J. Radiol. 2021, 141, 109804. [CrossRef]
78. Venkatesan, AM; Mudairu-Dawodu, E.; Duran, C.; Stafford, RJ; Yan, Y.; Wei, W.; Kundra, V. Rilevamento del cancro alla prostata ricorrente utilizzando la risonanza magnetica multiparametrica, l'influenza del PSA e del grado di Gleason. Imaging del cancro 2021, 21, 3. [CrossRef] [PubMed]
79. Panebianco, V.; Narumi, Y.; Altun, E.; Bochner, BH; Efstathiou, JA; Hafeez, S.; Huddart, R.; Kennish, S.; Lerner, S.; Montironi, R.; et al. Imaging a risonanza magnetica multiparametrica per il cancro della vescica: sviluppo di VI-RADS (Vesical Imaging-Reporting and Data System). Euro. Urol. 2018, 74, 294–306. [CrossRef]
80. Juri, H.; Narumi, Y.; Panebianco, V.; Osuga, K. Stadiazione del cancro alla vescica con risonanza magnetica multiparametrica. Fr. J. Radiol. 2020, 93, 20200116. [CrossRef]
81. Barua, SK; Kaman, PK; Barua, SJ; TP, R.; Bagchi, PK; Sarma, D.; Singh, Y. Ruolo della risonanza magnetica pesata in diffusione (DWMRI) nella valutazione delle caratteristiche primarie del tumore del pene e delle sue correlazioni con la metastasi dei linfonodi inguinali: uno studio prospettico. Mondo J.Oncol. 2018, 9, 145–150. [CrossRef]
82. Lindquist, CM; Nikolaidis, P.; Mittal, PK; Miller, FH MRI del pene. Addome. Radiol. 2020, 45, 2001–2017. [CrossRef]
83.Tsili, AC; Sofikitis, N.; Stiliara, E.; Argyropoulou, MI MRI di neoplasie testicolari. Addome. Radiol. 2019, 44, 1070–1082. [CrossRef] [PubMed]
84. Tsili, A. Valori del coefficiente di diffusione apparente e modelli di miglioramento del contrasto dinamico nel differenziare i seminomi dalle neoplasie testicolari nonseminomatose. Euro. J. Radiol. 2015, 84, 1219–1226. [CrossRef]
85 Moreno, CC; Piccolo, WC; Camacho, JC; Maestro, V.; Kokabi, N.; Lewis, M.; Hartmann, M.; Mittal, P. Tumori testicolari: cosa devono sapere i radiologi: diagnosi differenziale, stadiazione e gestione. Radiografia 2015, 35, 400–415. [CrossRef] [PubMed]
86. Parenti, GC; Feletti, F.; Carnevale, A.; Ucelli, L.; Giganti, M. Imaging dello scroto: oltre l'ecografia. Approfondimenti Imaging 2018, 9, 137–148. [CrossRef] [PubMed]
87.Tsili, AC; Bertolotto, M.; Turgut, AT; Dogra, V.; Libero, S.; Rocher, L.; Belfield, J.; Studniarek, M.; Ntorkou, A.; Derchi, LE; et al. Risonanza magnetica dello scroto: Raccomandazioni del gruppo di lavoro per l'imaging scrotale e penieno dell'ESUR. Euro. Radiol. 2018, 28, 31–43. [CrossRef] [PubMed]
88. Emad-Eldin, S.; Salim, AMA; Waba, MH; ElAhwany, AT; Abdelaziz, O. L'uso dell'imaging RM pesato in diffusione nella valutazione funzionale dei testicoli di pazienti con varicocele clinico. Andrologia 2019, 51, e13197. [CrossRef]
89. Ntorkou, A.; Tsili, CA; Goussia, A.; Astrakas, LG; Maliakas, V.; Sofikitis, N.; Argyropoulou, MI Coefficiente di diffusione apparente testicolare e rapporto di trasferimento della magnetizzazione: questi parametri MRI possono essere utilizzati per prevedere il recupero riuscito dello sperma nell'azoospermia non ostruttiva? Sono. J. Roentgenol. 2019, 213, 610–618. [CrossRef]
90. Caroli, A.; Schneider, M.; Friedli, I.; Ljimani, A.; De Seigneux, S.; Boor, P.; Gullapudi, L.; Kazmi, I.; Mendichovszky, IA; Notohamiprodjo, M.; et al. Risonanza magnetica pesata in diffusione per valutare la patologia renale diffusa: una revisione sistematica e un documento di dichiarazione. Nefrolo. Comporre. Trapianto. 2018, 33 (Suppl. S2), ii29–ii40. [CrossRef]
91. Jiang, K.; Ferguson, CM; Lerman, LO Valutazione non invasiva della fibrosi renale mediante tecniche di risonanza magnetica e ultrasuoni. Trad. Ris. 2019, 209, 105–120. [CrossRef]
92. Serter, A.; Onur, signor; Coban, G.; Yildiz, P.; Armagan, A.; Kocakoc, E. Il ruolo della risonanza magnetica pesata in diffusione e della risonanza magnetica con contrasto per la differenziazione tra masse renali solide e sottotipi di carcinoma a cellule renali. Addome. Radiol. 2021, 46, 1041–1052. [CrossRef] [PubMed]
93. Tordjman, M.; Mali, R.; Madelin, G.; Prabhu, V.; Kang, S. Precisione del test diagnostico dei valori ADC per l'identificazione del carcinoma a cellule renali a cellule chiare: revisione sistematica e meta-analisi. Euro. Radiol. 2020, 30, 4023–4038. [CrossRef] [PubMed]
94. Zhu, J.; Luo, X.; Gao, J.; Li, S.; Li, C.; Chen, M. Applicazione dell'imaging RM del tensore della curtosi di diffusione nella caratterizzazione dei carcinomi a cellule renali con diversi tipi e gradi patologici. Imaging del cancro 2021, 21, 30. [CrossRef] [PubMed]
95. Farhadi, F.; Nikpanah, M.; Paschall, AK; Shafiei, A.; Tadayoni, A.; Palla, PM; Linehan, WM; Jones, EC; Malayeri, la crescita del carcinoma a cellule renali a cellule chiare AA è correlata alla risonanza magnetica pesata in diffusione al basale nella malattia di Von Hippel-Lindau. Radiologia 2020, 295, 583–590. [CrossRef] [PubMed]
96. Goh, V.; Prezzi, D. Previsione della cinetica di crescita nel carcinoma renale ereditario con risonanza magnetica pesata in diffusione. Radiologia 2020, 295, 591–592. [CrossRef] [PubMed]
97. Vivier, P.-H.; Salem, A.; Beurdeley, M.; Lim, RP; Leroux, J.; Caudron, J.; Coudray, C.; Liardo, A.; Michelet, I.; Dacher, J.‑N. Risonanza magnetica e sospetta pielonefrite acuta nei bambini: confronto tra imaging pesato in diffusione e imaging pesato T 1- potenziato con gadolinio. Euro. Radiol. 2013, 24, 19–25. [CrossRef]
98. Thoeny, HC; De Keyzer, F. Imaging RM pesato in diffusione di reni nativi e trapiantati. Radiologia 2011, 259, 25–38. [CrossRef]
99. Faletti, R.; Cassini, MC; Fonio, P.; Grasso, A.; Battisti, G.; Bergamasco, L.; Gandini, G. Imaging pesato in diffusione e valori del coefficiente di diffusione apparente rispetto all'imaging RM potenziato dal contrasto nell'identificazione e caratterizzazione della pielonefrite acuta. Euro. Radiol. 2013, 23, 3501–3508. [CrossRef]
100. Sriman, R.; Venkatesh, K.; Matteo, C.; Pankaj, M.; Shankar, R. Validità della risonanza magnetica pesata in diffusione nella valutazione della pielonefrite acuta rispetto alla tomografia computerizzata con mezzo di contrasto. pol. J. Radiol. 2020, 85, e137–e143.
101. Aoyagi, J.; Kanai, T.; Odaka, J.; Ito, T.; Saito, T.; Betsui, H.; Furukawa, R.; Nakata, W.; Yamagata, T. Risonanza magnetica non potenziata rispetto alla scintigrafia renale nella pielonefrite acuta. Pediatr. Int. 2018, 60, 200–203. [CrossRef]
102. Bosáková, A.; Šalounová, D.; Havelka, J.; Kraft, O.; Sirucek, P.; Kocvara, R.; Hladik, M. La risonanza magnetica pesata in diffusione è più sensibile della scintigrafia con acido dimercaptosuccinico nel rilevare lesioni parenchimali nei bambini con pielonefrite acuta: uno studio prospettico. J. Pediatr. Urol. 2018, 14, 269.e1–269.e7. [CrossRef]
103. Simrén, Y.; Stokland, E.; Hansson, S.; Sixt, R.; Svensson, PA-A.; Lagerstrand, K. L'imaging pesato in diffusione è un metodo promettente per rilevare la pielonefrite acuta nei neonati a respirazione libera non sedati. J. Pediatr. Urol. 2020, 16, 320–325. [CrossRef] [PubMed]
104. Damasio, MB; Müller, L.-SO; Augdal, TA; Avni, FE; Basso, L.; Bruno, C.; Kljuˇcevšek, D.; Littoij, AS; Franchi-Abella, S.; Lobo, LM; et al. Task force per l'imaging addominale della Società europea di radiologia pediatrica: Raccomandazioni per l'ecografia con mezzo di contrasto e l'imaging pesato in diffusione nelle lesioni renali focali nei bambini. Pediatr. Radiol. 2019, 50, 297–304. [CrossRef] [PubMed]
105. Li, Y.; Lee, MM; Worters, PW; MacKenzie, JD; Laszik, Z.; Courtier, JL Pilot Study of Renal Diffusion Tensor Imaging come correlato all'istopatologia negli alloinnesti renali pediatrici. Sono. J. Roentgenol. 2017, 208, 1358–1364. [CrossRef] [PubMed]
106. Lanzmann, RS; Ljimani, A.; Pentang, G.; Zgoura, P.; Zenginli, H.; Kropil, P.; Heusch, P.; Schek, J.; Miese, Francia; Blondin, D.; et al. Trapianto di rene: valutazione funzionale con imaging RM a tensore di diffusione a 3T. Radiologia 2013, 266, 218–225. [CrossRef] [PubMed]
107. Hueper, K.; Gutberlet, M.; Rodt, T.; Vincitore, W.; Lehner, F.; Wacker, F.; Galansky, M.; Hartung, D. Imaging del tensore di diffusione e trattografia per la valutazione della disfunzione dell'allotrapianto renale: risultati iniziali. Euro. Radiol. 2011, 21, 2427–2433. [CrossRef] [PubMed]
108. Ventilatore, W.-J.; Affitto.; Li, Q.; Zuo, PL-L; Lungo, M.-M.; Mo, C.-B.; Chen, L.-H.; Huang, L.-X.; Shen, W. Valutazione della funzione dell'allotrapianto renale subito dopo il trapianto con imaging del tensore di diffusione a risoluzione isotropica. Euro. Radiol. 2015, 26, 567–575. [CrossRef]
109. Eisenberger, U.; Thoeny, HC; Binser, T.; Gugger, M.; Frey, FJ; Bosch, C.; Vermathen, P. Valutazione della funzione dell'allotrapianto renale subito dopo il trapianto con imaging RM pesato in diffusione. Euro. Radiol. 2010, 20, 1374–1383. [CrossRef]
110. Abou-El-Ghar, ME; El-Diasty, TA; El-Assmy, AM; Refaie, HF; Refaie, AF; Ghoneim, MA Ruolo della risonanza magnetica pesata in diffusione nella diagnosi di disfunzione acuta dell'allotrapianto renale: uno studio prospettico preliminare. Fr. J. Radiol. 2012, 85, e206–e211. [CrossRef]
111. Steiger, P.; Barbieri, S.; Kruse, A.; Ith, M.; Thoeny, HC Selezione per la biopsia di pazienti sottoposti a trapianto di rene mediante risonanza magnetica pesata in diffusione. Euro. Radiol. 2017, 27, 4336–4344. [CrossRef]
112. Ni, X.; Vanga, W.; Li, X.; Li, Y.; Chen, J.; Shi, D.; Wen, J. Utilità dell'imaging pesato in diffusione per guidare la gestione clinica dei pazienti con trapianto di rene: uno studio prospettico. J. Magn. Risonanza. Imaging 2020, 52, 565–574. [CrossRef]
113. Hussain, SM Editoriale per "Utilità dell'imaging pesato in diffusione per guidare la gestione clinica dei pazienti con trapianto di rene: uno studio prospettico". J. Magn. Risonanza. Imaging 2020, 52, 575–576. [CrossRef] [PubMed]
114. Chen, X.; Xiao, W.; Li, X.; Lui, J.; Huang, X.; Tan, Y. In vivo, valutazione della funzione renale mediante imaging pesato in diffusione e imaging del tensore di diffusione nei diabetici di tipo 2 con normoalbuminuria rispetto a microalbuminuria. Davanti. Med. 2014, 8, 471–476. [CrossRef] [PubMed]
115. Lu, L.; Sedor, Jr.; Gulani, V.; Schelling, Jr.; O'Brien, A.; Pallone, CA; Dell, KM Uso della risonanza magnetica del tensore di diffusione per identificare i primi cambiamenti nella nefropatia diabetica. Sono. J.Nephrol. 2011, 34, 476–482. [CrossRef] [PubMed]
116. Razek, AAKA; Al-Adlany, MAAA; Alhadidy, AM; Atva, MA; Abdou, NEA Imaging del tensore di diffusione della corteccia renale nei pazienti diabetici: correlazione con biomarcatori urinari e sierici. Addome. Radiol. 2017, 42, 1493–1500. [CrossRef]
117. Cakmak, P.; Yagci, AB; Dursun, B.; Herek, D.; Fenkci, SM Imaging pesato in diffusione renale nella nefropatia diabetica: correlazione con gli stadi clinici della malattia. Diagnostica. Interv. Radiol. 2014, 20, 374–378. [CrossRef]
118. Carbone, SF; Gaggioli, E.; Ricci, V.; Mazzei, F.; Mazzei, MA; Volterrani, L. Risonanza magnetica pesata in diffusione nella valutazione della funzione renale: uno studio preliminare. Radiol. Med. 2007, 112, 1201–1210. [CrossRef]
119. Ding, J.; Chen, J.; Jiang, Z.; Zhou, H.; Di, J.; Xing, W. Valutazione della disfunzione renale con imaging pesato in diffusione: confronto del movimento incoerente intra-voxel (IVIM) con un modello mono-esponenziale. Acta Radiol. 2015, 57, 507–512. [CrossRef]
120. Özçelik, Ü.; Çevik, H.; Bircan, HY; Karakayali, FY; I¸sıklar, I.; Haberal, M. Valutazione dei reni trapiantati e confronto con volontari sani e donatori di reni con risonanza magnetica pesata in diffusione: esperienza iniziale. Esp. Clino. Traspl. 2017. [CrossRef]
121. Emre, T.; Kiliçkesmez, Ö.; Buker, A.; Inale, BB; Do˘gan, H.; Ecder, T. Funzione renale e imaging pesato in diffusione: un nuovo metodo per diagnosticare l'insufficienza renale prima di perdere la metà della funzione. Radiol. Med. 2016, 121, 163–172. [CrossRef]
122. Xu, X.; Zanna, W.; Lin, H.; Chai, W.; Chen, K. Imaging RM pesato in diffusione dei reni in pazienti con malattia renale cronica: studio iniziale. Euro. Radiol. 2010, 20, 978–983. [CrossRef]
123. Yalçin-¸Safak, K.; Ayyildiz, M.; Ünel, SY; Umarusman-Tanju, N.; Akca, A.; Baysal, T. La relazione dei valori ADC del parenchima renale con lo stadio CKD e i livelli di creatinina sierica. Euro. J. Radiol. Aperto 2016, 3, 8–11. [CrossRef] [PubMed]
124. Liu H.; Zhou, Z.; Li, X.; Li, C.; Vanga, R.; Zhang, Y.; Niu, G. Imaging pesato in diffusione per la stadiazione della malattia renale cronica: una meta-analisi. Fr. J. Radiol. 2018, 91, 20170952. [CrossRef] [PubMed]
125. Beck-Tolly, A.; Eder, M.; Beitzke, D.; Eskandary, F.; Agibetov, A.; Lampichler, K.; Hambock, M.; Regele, H.; Klager, J.; Nackenhorst, M.; et al. Imaging a risonanza magnetica per la valutazione della fibrosi interstiziale negli alloinnesti renali. Traspl. Diretto 2020, 6, e577. [CrossRef] [PubMed]
126. Berchtold, L.; Crowe, Los Angeles; Combescure, C.; Kassaï, M.; Aslam, I.; Legouis, D.; Molly, S.; Martin, P.-Y.; de Signore, S.; Vallée, J.‑P. La risonanza magnetica in diffusione predice il declino della funzione renale nella malattia renale cronica e nei pazienti con un allotrapianto di rene. Rene Int. 2022, 101, 804–813. [CrossRef] [PubMed]
127. Berchtold, L.; Friedli, I.; Crowe, Los Angeles; Martinez, C.; Molly, S.; Hadaya, K.; De Perrot, T.; Combescure, C.; Martin, P.-Y.; Vallée, J.-P.; et al. Convalida della differenza corticomidollare nel coefficiente di diffusione apparente derivato dalla risonanza magnetica per il rilevamento della fibrosi renale: uno studio trasversale. Nefrolo. Comporre. Traspl. 2020, 35, 937–945. [CrossRef]
128. Buchanan, CE; Mahmud, H.; Cox, FE; McCulloch, T.; Prestwich, BL; Tal, MW; Selby, N.; Francis, ST Valutazione quantitativa dei cambiamenti strutturali e funzionali renali nella malattia renale cronica mediante risonanza magnetica multiparametrica. Nefrolo. Comporre. Traspl. 2019, 35, 955–964. [CrossRef]
129. Friedli, I.; Crowe, Los Angeles; Berchtold, L.; Molly, S.; Hadaya, K.; De Perrot, T.; Vesino, C.; Martin, P.-Y.; De Seigneux, S.; Vallée, J.‑P. Nuovo indice di imaging a risonanza magnetica per la valutazione della fibrosi renale: un confronto tra imaging pesato in diffusione e mappatura T1 con convalida istologica. Sci. Rep. 2016, 6, 30088. [CrossRef]
130. Inoue, T.; Kozawa, E.; Okada, H.; Inukai, K.; Watanabe, S.; Kikuta, T.; Watanabe, Y.; Takenaka, T.; Katayama, S.; Tanaka, J.; et al. Valutazione non invasiva dell'ipossia e della fibrosi renale mediante risonanza magnetica. Marmellata. soc. Nefrolo. 2011, 22, 1429–1434. [CrossRef]
131. Mao, W.; Ding, Y.; Ding, X.; Fu, C.; Zeng, M.; Zhou, J. Imaging della curtosi da diffusione per la valutazione della fibrosi renale della malattia renale cronica: uno studio preliminare. Magn. Risonanza. Imaging 2021, 80, 113–120. [CrossRef]
132. Zhang, J.; Yu, Y.; Liu, X.; Tang, X.; Xu, F.; Zhang, M.; Xi, G.; Zhang, L.; Li, X.; Liu, Z-H. Valutazione della fibrosi renale mediante mappatura istologica e risonanza magnetica. Rene Dis. 2021, 7, 131–142. [CrossRef]
133. Zhao, J.; Wang, Z.; Liu, M.; Zhu, J.; Zhang, X.; Zhang, T.; Li, S.; Li, Y. Valutazione della fibrosi renale nella malattia renale cronica mediante risonanza magnetica pesata in diffusione. Clino. Radiol. 2014, 69, 1117–1122. [CrossRef] [PubMed]
134. Akashi, t.; Terayama, N.; Okada, E. Lesione pelvica renale solitaria come manifestazione primaria del linfoma di Hodgkin: un caso clinico. Urol. Caso Rep. 2017, 13, 87–88. [CrossRef] [PubMed]
135. Liu Y.; Zhang, G.-M.-Y.; Peng, X.; Li, X.; Sole, H.; Chen, L. Imaging della curtosi da diffusione come biomarcatore di imaging per la previsione della prognosi nei pazienti con malattia renale cronica. Nefrolo. Comporre. Traspl. 2021, gfab229. [CrossRef] [PubMed]
136. Srivastava, A.; Cai, X.; Lee, J.; Li, W.; Larive, B.; Kendrick, C.; Gassmann, JJ; Middleton, Giappone; Carr, J.; Raffaello, KL; et al. Risonanza magnetica funzionale del rene e variazione dell'eGFR in individui con insufficienza renale cronica. Clino. Marmellata. soc. Nefrolo. 2020, 15, 776–783. [CrossRef]
137. Ljimani, A.; Caroli, A.; Laustsen, C.; Francesco, S.; Mendichovszky, IA; Bane, O.; Neri, F.; Sharma, K.; Pohlmann, A.; Dekker, AI; et al. Raccomandazioni tecniche basate sul consenso per la traduzione clinica della risonanza magnetica pesata in diffusione renale. Magn. Risonanza. Madre. Fis. Biol. Med. 2020, 33, 177–195. [CrossRef]
Thomas De Perrot 1, Christine Sadjo Zoua 1, Carl G. Glessgen 1, Diomidis Botsikas 1, Lena Berchtold 2, Rares Salomir 1, Sophie De Seigneux 2, Harriet C. Thoeny 3 e Jean-Paul Vallée 1
1 Divisione di Radiologia, Ospedali Universitari di Ginevra e Università di Ginevra, 1205 Ginevra, Svizzera; christine.sadjo@hcuge.ch (CSZ); carl.glessgen@hcuge.ch (CGG); diomidis.botsikas@hcuge.ch (DB); raresvincent.salomir@hcuge.ch (RS); Jean-paul.vallee@hcuge.ch (J.-PV)
2 Divisione di Nefrologia, Ospedali universitari di Ginevra, 1205 Ginevra, Svizzera; lena.berchtold@hcuge.ch (LB); sophie.deseigneux@hcuge.ch (SDS)
3 Divisione di Radiologia, Hôpital Cantonal Fribourgois, 1752 Villars-sur-Glâne, Svizzera; harriet.thoeny@h-fr.ch






