Effetti protettivi della wogonin sull'infammazione indotta da lipopolisaccaridi e sull'apoptosi delle cellule epiteliali polmonari e sui suoi possibili meccanismi
Mar 18, 2022
Contattotina.xiang@wecistanche.com
Astratto
Sfondo: La wogonin (5,7-diidrossi-8-metossiflavone) è un flavonoide diidrossilico naturale estratto dalla radice di Scutellaria baicalensis Georgi. Questo articolo aveva lo scopo di indagare il meccanismo d'azione della wogonin nell'alleviareinfiammazioneeapoptosinel danno polmonare acuto (ALI).
Materiali e metodi: Il lipopolisaccaride (LPS) è stato utilizzato per stabilire il modello in vitro di ALl. Dopo il trattamento con wogonin, la vitalità cellulare e l'apoptosi delle cellule A549 indotte da LPS sono state, rispettivamente, misurate mediante CCK-8, TUNELassays e doppia colorazione di acridina arancione/bromuro di etidio, mentre il contenuto di citochine infiammatorie elo stress ossidativoi marcatori sono stati stimati mediante RT-qPCR, test ELISA, analisi western blot e kit commerciali. Il western blot è stato anche condotto per valutare l'espressione delle proteine coinvolte. Successivamente, è stato studiato l'effetto della wogonin sulla deacetilazione della proteina box 1 (HMGB1) mediata da sirtuin 1 (SIRT1) mediata da sirtuin 1 (SIRT1). L'inibitore SIRT1 EX527 è stato utilizzato per valutare gli effetti regolatori della wogonin sulla deacetilazione HMGB1 mediata da SIRT1- nelle cellule A549 sotto stimolazione LPS.
Risultati: LPS ha indotto infiammazione, stress ossidativo e apoptosi delle cellule A549, che è stata abolita dalla wogonin. È stato anche scoperto che la wogonin promuoveva la deacetilazione di HMGB1, accompagnata da un'espressione SIRT1 sovraregolata. Tuttavia, l'inibitore SIRT1 EX527 ha parzialmente invertito gli effetti protettivi della wogonin sull'infiammazione e l'apoptosi delle cellule A549 indotte da LPS.
Conclusione: Wogonin ha alleviato l'infiammazione e l'apoptosi nelle cellule A549 indotte da LPS mediante la deacetilazione HMGB1 mediata da SIRT1-, che potrebbe rappresentare l'identificazione di un nuovo meccanismo mediante il quale la wogonin esercita effetti protettivi sull'ALI e fornire idee per l'applicazione della wogonin a TUTTO il trattamento.
Parole chiave: Danno polmonare acuto, Wogonin, Infiammazione, SIRT1, deacetilazione HMGB1

Clicca qui per ulteriori informazioni
Sfondo
Il danno polmonare acuto (AL) è clinicamente documentato come il risultato di stati patologici tra cui sepsi, polmonite, traumi e pancreatite acuta [1]. Si osserva spesso nei pazienti ricoverati nelle unità di terapia intensiva e mostra un alto tasso di mortalità [2]. Coloro che sopravvivono all'ALI si trovano solitamente di fronte a una qualità di vita inferiore [3]. Sebbene siano stati raggiunti risultati nella comprensione della fisiopatologia dell'AL, l'efficacia del trattamento delle attuali terapie rimane limitata, il che non può soddisfare le aspettative dei pazienti e delle loro famiglie [4]. Pertanto, è di grande urgenza identificare nuove terapie o obiettivi per il trattamento di ALL. Il wogonin(5,{5}}diidrossi{6}}metossiflavone), la cui struttura è mostrata in Fig.1A, è un flavonoide diidrossile naturale estratto dalla radice di Scutellaria baicalensis Georgi [5]. Le sue notevoli proprietà antinfiammatorie e la sua applicazione nel trattamento delle malattie infiammatorie sono state ampiamente riportate da un gran numero di studi. Ad esempio, la wogonin ha potenzialmente migliorato l'edema polmonare nei murini e li ha protetti dall'ALI indotta da lipopolisaccaridi (LPS) bloccando la protein chinasi attivata dal mitogeno p38 (MAPK) e la chinasi terminale c-Jun NH(2) (fosforilazione INK [6] La wogonin ha anche ridotto l'infiltrazione dei neutrofili indotta da LPS, la produzione di citochine proinfiammatorie, l'espressione di molecole di adesione e la soppressione di AL indotta da LPS nei topi. risultato del trattamento con wogonin mediante la via NF-KB mediata dal recettore gamma(PPARy) attivato dal proliferatore del perossisoma [8] Lo studio emergente ha dimostrato che la wogonin riduce la legatura cecale e la puntura (CLP) indotta dalla proteina box 1 del gruppo ad alta mobilità (HMGB1) produzione e infiammazione dipendente da HMGB1-, e riduzione della morbilità correlata alla sepsi e del rischio di danno polmonare [9]. Nel modello ALI in vitro e in vivo indotto da LPS, un altro rapporto ha dimostrato che l'inibizione di HMGB1 e altri mediatori dell'infiammazione tramite l'ulinastatina hanno evidentemente alleviato le manifestazioni di ALI [10]. E studi precedenti hanno confermato che le cellule epiteliali polmonari umane indotte da LPS (A549) sono state ampiamente utilizzate come modello in vitro per ALI [11-13]. È stato suggerito che Sirtuin 1 (SIRT1), l'effettore a valle della protein chinasi attivata da adenosina monofosfato (AMPK), svolga un ruolo significativo nella regolazione del rilascio di adiponectina [14]. La supplementazione di wogonin ha notevolmente aumentato la fosforilazione di AMPK e l'espressione di SIRT1, mentre l'inibizione di AMPK o SIRT1 ha ridotto gli effetti della wogonin sulla produzione o sul rilascio di adiponectina [14]. In precedenza era stato riportato che la deacetilazione dell'HMGB1 modulata da SIRT1- inibiva il danno renale acuto causato dalla sepsi [15].
Nel presente studio, abbiamo mirato a studiare il meccanismo d'azione della wogonin nell'alleviare ilinfiammazioneeapoptosidi cellule epiteliali polmonari umane indotte da LPS, che potrebbero fornire una visione più completa per il trattamento dell'ALI da parte della wogonin.

Risultati
Effetti della wogonin sulla vitalità e l'apoptosi delle cellule A549 indotte da LPS
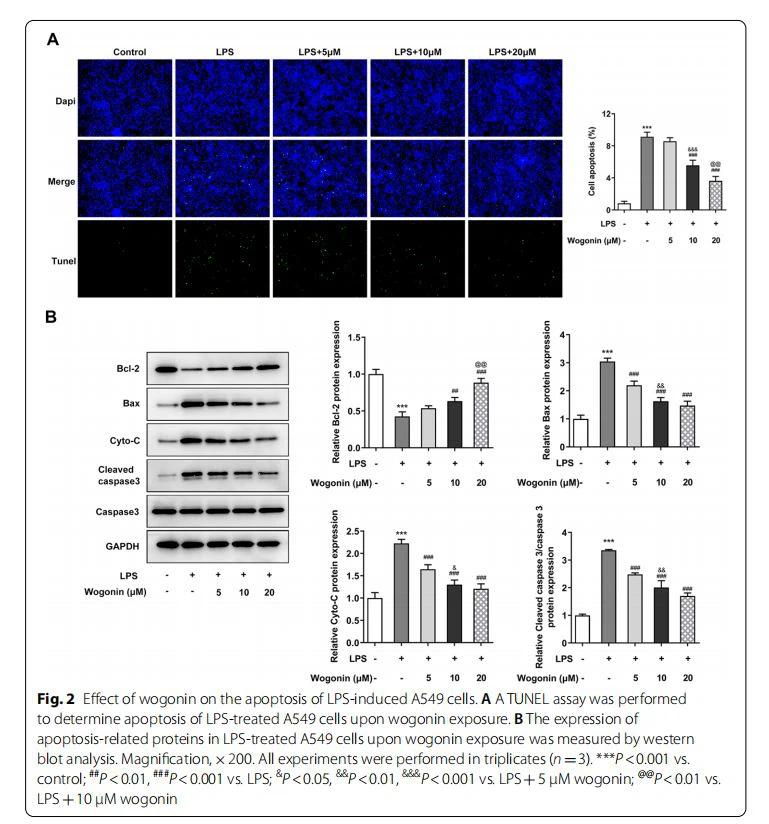
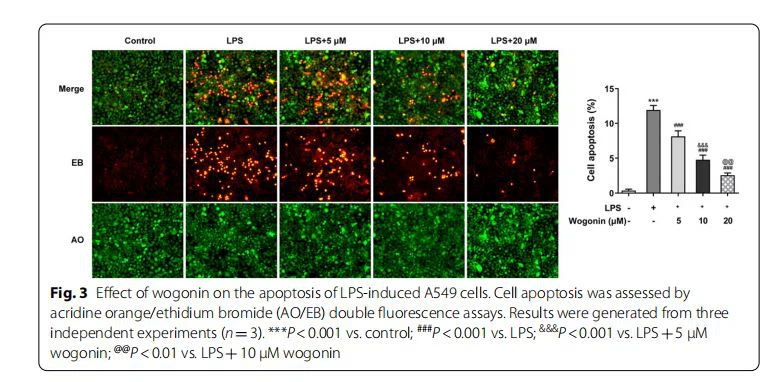
Per osservare l'effetto della wogonin sull'ALI, abbiamo prima ipotizzato se la vitalità delle normali cellule A549 potesse essere danneggiata dalla wogonin. Come mostrato in Fig. 1B, la wogonin non ha danneggiato le cellule A549 senza ricevere alcun trattamento, suggerendo la sicurezza del trattamento con wogonin nelle cellule A549 alle concentrazioni di O,5,10 e 20 μM. Dopo la stimolazione con LPS per 24 ore, la vitalità delle cellule A549 è stata notevolmente danneggiata, che è stata contrastata dalla wogonin in modo dipendente dalla concentrazione (Fig. 1C). Inoltre, i risultati del test LDH hanno mostrato che un aumento significativo dell'attività LDH nelle cellule A549 trattate con LPS è stato ridotto dopo la somministrazione di dosi crescenti di wogonin (Fig. 1D). Successivamente, abbiamo testato l'effetto della wogonin sull'apoptosi delle cellule A549 indotte da LPS. Come mostrato in Fig.2A, la colorazione TUNEL ha dimostrato che l'esposizione a LPS ha migliorato notevolmente l'apoptosi delle cellule A549 rispetto al gruppo di controllo, che è stata ridotta dalla wogonin in modo dose-dipendente. Inoltre, nel gruppo esposto a LPS sono state osservate un'apparente sottoregolazione nell'espressione di Bcl-2 e una sovraregolazione nelle espressioni Bax, Cyto-C e caspasi 3 scissa rispetto al gruppo di controllo, che è stato ripristinato dal trattamento con wogonin (Fig. 2B). Coerentemente, i risultati dei saggi a doppia fluorescenza AO/EB presentati in Fig.3 hanno suggerito che l'LPS ha portato a un tasso di apoptosi cellulare elevato rispetto al gruppo di controllo, mentre le cellule EB-positive sono state notevolmente ridotte dopo l'aggiunta di wogonin rispetto all'LPS gruppo. Pertanto, la wogonin ripristina la vitalità e riduce l'apoptosi delle cellule A549 indotte da LPS.
Effetti della wogonin sull'infiammazione e sullo stress ossidativo delle cellule A549 indotte da LPS
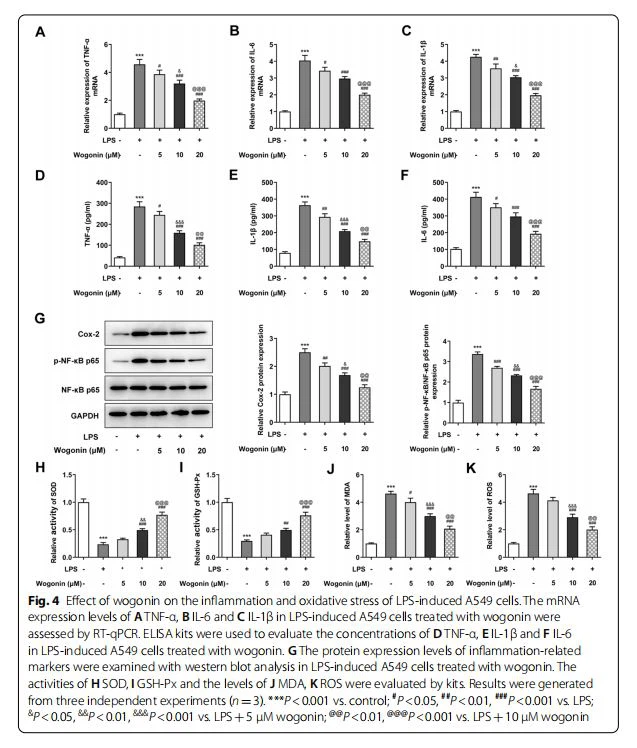
Per esplorare le capacità antinfiammatorie e antiossidanti della wogonin in ALI, ilinfiammazioneelo stress ossidativodelle cellule A549 indotte da LPS trattate con wogonin sono state, rispettivamente, rilevate. Come si vede in Fig. 4A-C, i livelli di mRNA delle citochine infiammatorie (TNF-, IL-6 e IL-1) misurati mediante RT-qPCR sono aumentati a livelli notevolmente elevati dopo la stimolazione con LPS, mentre la wogonin il trattamento ha portato alla riduzione della loro espressione. Coerentemente, i risultati dell'ELISA hanno indicato che l'induzione di LPS ha portato a un aumento significativo dei contenuti di TNF-, IL-6 e IL-1 rispetto al gruppo non trattato, che erano diminuiti in modo dose-dipendente dopo il trattamento con wogonin (Fig. .4D-F). È importante sottolineare che la ciclossigenasi-2(Cox-2) e il fattore fosfonucleare (NF)-KB p65 (p-NF-KB p65), che sono marcatori correlati all'infiammazione, sono stati sottoregolati da LPS mentre sovraregolato dalla wogonin (Fig. 4G). Inoltre, LPS ha comportato una diminuzione delle attività di SOD e GSH-Px e un aumento del contenuto di MDA e ROS, che è stato invertito dalla wogonin (Fig. 4H-K). Presi insieme, la wogonin allevia l'infiammazione e lo stress ossidativo delle cellule A549 indotte da LPS.

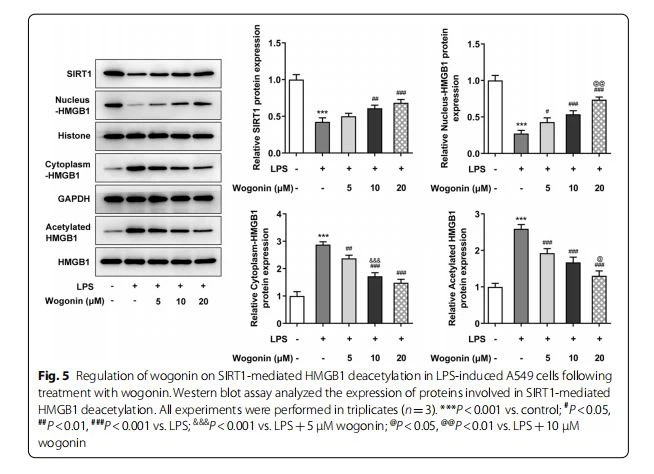
Regolazione della wogonin nella deacetilazione HMGB1 mediata da SIRT1-
Per confermare la nostra ipotesi che la wogonin abbia esercitato effetti protettivi sul danno cellulare A549 indotto da LPS da parte della deacetilazione HMGB1 mediata da SIRT1-, abbiamo eseguito il western blot per rilevare i livelli proteici dei fattori coinvolti. Evidentemente, LPS ha soppresso l'espressione di SIRT1 e ha promosso la traslocazione di HMGB1 dal nucleo al citoplasma, insieme all'acetilazione di HMGB1. Tuttavia, questa tendenza è stata invertita dall'esposizione alla wogonina alle cellule A549 indotte da LPS (Fig.5). Pertanto, il trattamento con wogonin regola la deacetilazione HMGB1 mediata da SIRT1-nelle cellule A549 indotte da LPS.
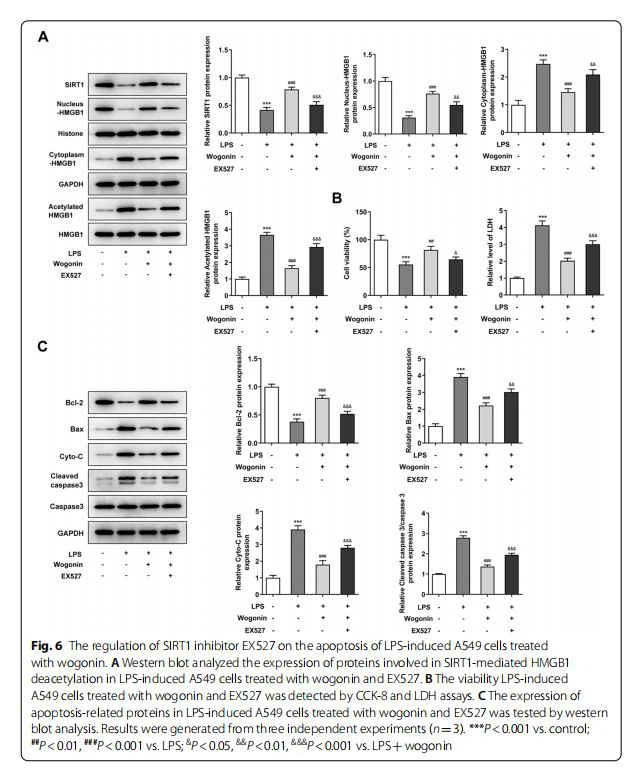
La regolazione dell'inibitore SIRT1 EX527 sui comportamenti cellulari delle cellule A549 indotte da LPS trattate con wogonin
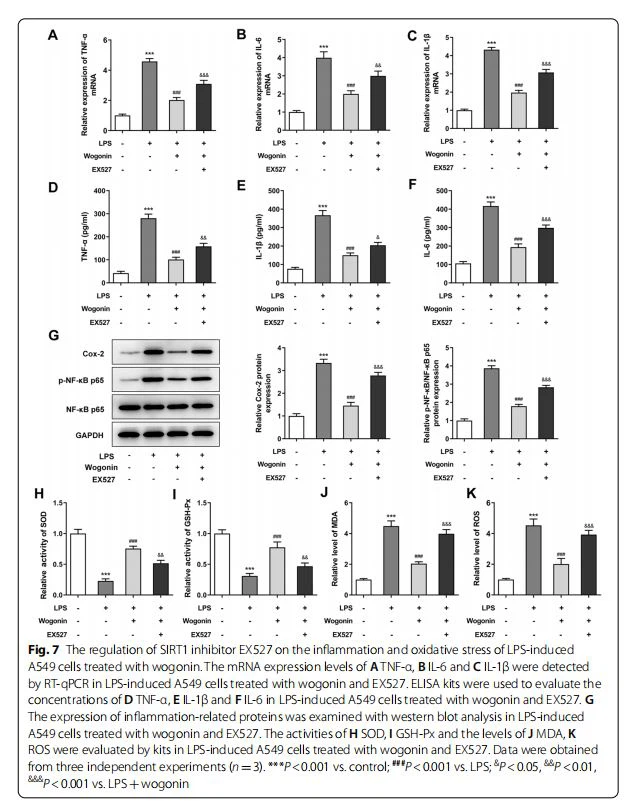
Per verificare il ruolo di SIRT1 nel meccanismo sottostante mediante il quale la wogonin ha influenzato l'infiammazione e l'apoptosi delle cellule A549 indotte da LPS, abbiamo usato EX527, un inibitore di SIRT1, per trattare le cellule A549 indotte da LPS per 24 ore. Come mostrato in Fig.6A, l'aggiunta di EX527 ha ridotto l'espressione di SIRT1, ha impedito il trasporto nucleo-citoplasmatico di HMGB1 e ha stimolato la deacetilazione di HMGB1, rispetto al gruppo LPS più Wogonin. Ulteriori test CCK-8 e LDH hanno mostrato che EX527 ha danneggiato l'effetto riparativo della wogonin sulla vitalità delle cellule A549 indotte da LPS (Fig.6B). Inoltre, gli effetti della wogonin sull'espressione di Bcl-2, Bax, Cyto-C e l'espressione della caspasi 3 scissa sono stati in parte alleviati da EX527 nelle cellule A549 indotte da LPS (Fig.6C). Infine, le tendenze di variazione dei fattori infiammatori (TNF- , IL-6 e IL-1 ), delle proteine correlate all'infiammazione (Cox-2 e p-NF-kB p65) e marcatori di stress ossidativo (SOD, GSH-Px e MDA) nelle cellule A549 indotte da LPS co-trattate con wogonin ed EX527 hanno dimostrato che EX527 ha danneggiato gli effetti inibitori della wogonin sull'infiammazione e lo stress ossidativo nelle cellule A549 indotte da LPS (Fig. 7A-K). Pertanto, l'inibitore SIRT1 EX527 inverte gli effetti protettivi della wogonin sui fenotipi maligni delle cellule A549 indotte da LPS.
Discussione
Attualmente, molti esperti hanno riconosciuto la wogonin come un potente agente per il trattamento delle malattie infiammatorie. Secondo quanto riferito, la sua efficacia nell'alleviare le risposte infiammatorie è stata attribuita alla soppressione di NF-kB e all'attivazione delle vie di segnalazione del fattore 2(Nrf2) correlato al fattore nucleare eritroide 2-[16]. È interessante notare che i precedenti rapporti associavano l'effetto antinfiammatorio alla mediazione dell'espressione di iNOS e Cox-2 o all'attivazione di vie di segnalazione di specie reattive dell'ossigeno (ROS)/ERK/Nrf2 [5,17]. Coerentemente con i risultati precedenti che non mostravano alcun effetto della wogonin sulla vitalità dei condrociti, non abbiamo trovato praticamente alcun effetto citotossico significativo della wogonin sulle normali cellule A549, supportando la nostra ulteriore esplorazione del meccanismo sottostante mediante il quale la wogonin ha influenzato il modello cellulare ALI in vitro [17]. Lo stress ossidativo e l'infiammazione sono due dei principali segni distintivi nella patogenesi di AL, e quindi abbiamo rilevato i cambiamenti negli indicatori di stress ossidativo e nelle citochine infiammatorie durante il trattamento con wogonin [18]. È interessante notare che l'infiammazione e lo stress ossidativo sono stati entrambi alleviati dall'esposizione alla wogonina nel modello cellulare A549 trattato con LPS, come evidenziato dal blocco del rilascio del fattore pro-infiammatorio e dalla maggiore produzione di SOD e GSH-Px, nonché dalla diminuzione della produzione di MDA dopo trattamento con wogonin HMGB1 emerge come una proteina altamente conservata che è stata identificata per la prima volta per modulare la sepsi in un modello murino[19]. Il targeting di HMGB1 è stato considerato una potenziale opzione terapeutica per il trattamento della sepsi, poiché i pazienti che si manifestavano come risposte infiammatorie prolungate mostravano frequentemente livelli elevati di HMGB1 continui [10]. Rapporti e revisioni recenti hanno prestato molta attenzione agli effetti terapeutici di HMGB1 sulle malattie infiammatorie, non limitate alla sepsi. Ad esempio, è stato precedentemente dimostrato che l'inibizione di HMGB1 da parte dell'ulinastatina ha migliorato il danno ALI indotto da LPS nei topi [10,20]. Dopo essere stato rilasciato da monociti/macrofagi attivati, HMGB1 è servito come fattore proinfiammatorio attraverso vari stimolanti [20]. Segnali infiammatori come LPS potrebbero indurre la traslocazione correlata all'acetilazione di HMGB1 dal nucleo al citoplasma [21]. Qui, la scoperta che la traslocazione di HMGB1 dal nucleo al citoplasma dopo la stimolazione dell'LPS è stata contrastata dal trattamento con wogonin ha chiarito indirettamente che l'infiammazione delle cellule A549 innescata dall'LPS è stata fortemente ostacolata dalla wogonin.
È stato suggerito che SIRT1 svolga un ruolo significativo in vari processi biologici [22]. A seconda dei suoi bersagli di deacetilazione, le alterazioni nell'attività di SIRT1 erano presumibilmente legate allo stress ossidativo e all'infiammazione [23]. HMGB1 è stato recentemente riconosciuto come bersaglio di deacetilazione di SIRT1 [20]. Prove sostanziali hanno indicato che la deacetilazione modulata da SIRT1- di HMGB1 ha alleviato l'infiammazione, ripristinato la funzione renale e prolungato il tempo di sopravvivenza dei topi con danno renale acuto correlato alla sepsi [15]. In uno studio sperimentale sulla lesione cerebrale traumatica, l'acido grasso polinsaturo Omega-3 ha alleviato l'infiammazione modulando la polarizzazione della microglia attraverso la deacetilazione modulata SIRT1- della via HMGB1/NF-KB [24]. Inoltre, l'acido oleanolico ha impedito al modello di ratto di emorragia subaracnoidea mediante la deacetilazione HMGB1 modulata da SIRT1-[25]. L'inibizione di NLRP3/NF-kB da parte dell'aloina tramite l'attivazione di SIRT1 ha attenuato l'ALI sfidata da LPS nei topi [26]. Regolando la segnalazione SIRT1/HMGB1/NF-KB, il kaempferolo ha migliorato il danno polmonare indotto dall'ischemia-riperfusione attraverso lo stress antinfiammatorio e antiossidante 27I. In quanto importante molecola a valle di HMGB1, NF-kB è una delle principali vie di segnalazione coinvolte nella regolazione dei mediatori dell'infiammazione attivando i geni dei fattori proinfiammatori e rilasciando un gran numero di fattori infiammatori, tra cui TNF-, IL-6 e TNF -a[28,29]. Inoltre, NF-KB può anche partecipare al processo di stress ossidativo regolando la produzione di ROS e influenzando i livelli di SOD, MDA e GSH-Px [30]. Nel presente studio, il è stata osservata una ridotta espressione di p-NF-kB p65 dopo l'aggiunta di wogonin, che è stata ripristinata dall'inibitore SIRT1, EX527. Inoltre, abbiamo scoperto che l'HMGB1 deacetilato dalla wogonin era accompagnato dall'espressione di SIRT1 attivata, il che ha portato alla nostra ipotesi che la wogonin possa esercitare effetti protettivi sull'infiammazione indotta da LPS delle cellule A549 dalla deacetilazione dell'HMGB1 mediata da SIRT1-. L'uso di EX527 nei seguenti esperimenti ha ulteriormente dimostrato che l'inibizione di SIRTl ha invertito gli effetti protettivi della wogonin sull'infiammazione delle cellule A549 indotte da LPS.

Conclusione
In conclusione, abbiamo dimostrato che la wogonin ha alleviato l'infiammazione, lo stress ossidativo e l'apoptosi del modello cellulare ALI indotto da LPS. Questo meccanismo d'azione sembrava essere dovuto alla regolazione della deacetilazione dell'HMGB1 mediata da SIRT1- innescata dalla wogonin. Questi risultati potrebbero identificare un nuovo meccanismo mediante il quale la wogonin esercita effetti protettivi sull'ALI e fornire una base sperimentale per l'applicazione della wogonin al trattamento clinico dell'ALI.
Materiali e metodi
Colture cellulari e farmaci
Human lung epithelial cells(A549) were purchased from the Cell Bank of Shanghai Institute of Biochemistry and Cell Biology at the Chinese Academy of Sciences (Shanghai, China) and cultured in Dulbecco's Modified Eagle Medium (DMEM; Gibco, Paisley, UK) containing 10% heat-inactivated fetal bovine serum(Gibco, Paisley, UK), 100 U/ml penicillin, and 100 g/ml streptomycin at 37 ℃ with 5% CO. The cells were collected after 10 μg/mL LPS(Sigma Chemical Co., St Louis, MO)stimulation for 24 h. Wogonin (purity>Il 99 per cento), isolato da Scutellaria baicalensis Georgi, è stato acquistato da Biotic Chemical (Taipei, Taiwan). È stato sciolto in dimetilsolfossido (DMSO), conservato a -20 grado C e diluito con DMEM. SIRT1 inibitore EX527(10 μM; MedChemExpress, Shanghai, Cina) è stato utilizzato per trattare le cellule per 24 ore prima della somministrazione secondo lo studio precedente [31].
Test del kit per il conteggio delle cellule-8 (CCK-8).
Dopo la stimolazione di LPS per 24 ore e varie concentrazioni di esposizione alla wogonina per altre 4 ore, le cellule sono state seminate in una piastra a pozzetti 96- ed è stato eseguito il test di vitalità cellulare aggiungendo 10μL di reagente CCK-8(Dojindo , Kumamoto, Giappone) in ciascun pozzo a 37 gradi per 4 h. L'assorbanza a 450 nm è stata monitorata utilizzando un lettore di micropiastre (Bio-Rad Laboratories, Inc.).
Saggio di rilascio della lattato deidrogenasi (LDH).
Il surnatante cellulare trattato con wogonin è stato seminato in 96-piastre di coltura a pozzetti e incubato per 24 ore a 37 gradi con il 5% di CO, prima di aggiungere 100 μL della soluzione LDH del kit di rilevamento della citotossicità (Roche Diagnostics, Francia) a ciascuna bene.15 minuti dopo, il surnatante cellulare è stato diluito, con il valore di densità ottica monitorato a 450 nm.
Il test TUNEL di colorazione dell'etichettatura dell'estremità del nick (TUNEL) mediato dalla deossinucleotidil transferasi terminale è stato effettuato per valutare l'apoptosi delle cellule A549 indotte da LPS con o senza trattamento con wogonin mediante il kit colorimetrico TUNEL Apoptosis Assay Kit (Beyotime, Shanghai, Cina) basato sull'operazione linee guida. Dopo il lavaggio con tampone fosfato salino (PBS) due volte e la fissazione con paraformaldeide al 4% per 0.5 h,0.3% di perossido di idrogeno in PBS è stato utilizzato per incubare le cellule per altri 20 minuti a temperatura ambiente. Le cellule sono state quindi trattate con diaminobenzene (DAB) per 10 minuti e controcolorate con ematossilina (Solarbio, Pechino, Cina) per 30 s. Le cellule apoptotiche-positive sono state osservate da un microscopio a fluorescenza (Olympus Corporation) e il tasso di apoptosi è stato qualificato dal software Image-J (NIH, Bethesda, MD, USA).
Doppia colorazione arancio acridina/bromuro di etidio
Sono stati eseguiti saggi a doppia fluorescenza di acridina/bromuro di etidio (AO/EB) per valutare l'alterazione dell'apoptosi cellulare. In breve, le cellule A549 sono state coltivate su vetrini coprioggetto in 24-piastre a pozzetti. Le cellule sono state preincubate per 24 ore con terreno privo di siero e quindi incubate con LPS e varie concentrazioni di wogonin a 37°C. Le cellule sono state lavate con PBS e fornite con 5μL di soluzione mista AO/EB (100 ug/ml di AO e 100 ug/ml di EB mescolati in PBS, Aladdin, Cina) entro 3 min. Le cellule sono state osservate e scattate una fotografia alla lunghezza d'onda di eccitazione di 510 nm al microscopio a fluorescenza (Olympus Corporation).
Analisi Western blot
Le proteine sono state estratte dalle cellule A549 utilizzando il tampone di lisi RIPA (Beyotime, Shanghai, Cina) e le concentrazioni di proteine sono state misurate mediante un kit di analisi delle proteine dell'acido bicinconinico (BCA) (Thermo Fisher Scientific, USA). Successivamente, è stata eseguita l'elettroforesi su gel di elettroforesi di sodio dodecil solfato-poliacrilammide (SDS-PAGE) per separare 40 ug di proteine e le proteine sono state quindi trasferite su membrane di polivinilidene difluoruro (PVDF). Queste membrane sono state quindi bloccate da latte scremato e quindi incubate a 4 gradi C durante la notte con anticorpi primari. Successivamente, l'anticorpo secondario coniugato con HRP è stato utilizzato per incubare le membrane per 1,5 ore a temperatura ambiente. Infine, le bande sono state visualizzate da un kit di chemiluminescenza (ECL) potenziato (Amersham Biosciences, Buckinghamshire, Regno Unito), mentre l'intensità della banda è stata monitorata utilizzando il software Image-J (NIH, Bethesda, MD, USA). GAPDH è stato considerato un riferimento interno.
PCR quantitativa della trascrizione inversa (RT-gPCR)
Le cellule A549 sono state lisate in 1 ml di reagente TRIzol (Invitrogen, Carlsbad, CA, USA) per l'estrazione dell'RNA totale. Dopo la raccolta dell'RNA totale, è stata condotta la trascrizione inversa per la sintesi del DNA complementare (cDNA) mediante il kit di reagenti PrimeScript RT (Takara Bio, Inc.). Le condizioni erano le seguenti: 50 gradi C per 15 minuti, 85 gradi C per 5 secondi, e conservazione a 4 gradi .SYBR Premix Ex Taq TM (TaKaRa, Giappone) è stato utilizzato per impostare le condizioni di reazione della PCR e il sistema di reazione in base ai suggerimenti del produttore. Per la qPCR è stato utilizzato uno strumento ABI 7500 (AB-4351107; Applied Biosystems; Thermo Fisher Scientific, Inc.). Sono state utilizzate le seguenti condizioni di termociclaggio: denaturazione iniziale a 95 gradi per 10 min; seguiti da 40 cicli di denaturazione a 95 gradi C per 15 s e ricottura a 60 gradi per 1 min; e un'estensione finale di 10 minuti a 72 gradi C. GAPDH è stato accettato come controllo di normalizzazione dell'espressione genica relativa. Il calcolo dell'espressione genica relativa è stato condotto con il metodo 2-AAct.
Saggio di immunoassorbimento enzimatico (ELISA)
I livelli cellulari di interleuchina-6(IL-6), IL-1 e fattore di necrosi tumorale- (TNF-) nel surnatante cellulare sono stati misurati utilizzando IL{5}} ELISA Kit , IL-1 ELISA Kit e TNF-ELISA Kit sulla base dei suggerimenti del produttore (Shanghai Xi Tang Biotechnology, Shanghai, Cina).
Rilevazione dello stress ossidativo
Per il rilevamento dello stress ossidativo, le attività dei marcatori di stress ossidativo tra cui malondialdeide (MDA), specie reattive dell'ossigeno (ROS), glutatione perossidasi (GSH-Px) e superossido dismutasi (SOD) sono state rilevate seguendo le istruzioni del produttore (Nanjing Jiancheng Biotechnology Istituto, Cina).
analisi statistica
Tutti i dati sono stati mostrati come media ± deviazione standard (SD) di almeno tre esperimenti indipendenti. Per i confronti tra più gruppi, è stata eseguita l'analisi della varianza unidirezionale (ANOVA) con il test post hoc di Tukey, mentre quelli tra due gruppi sono stati condotti dal test t di Student. P<0.05 was="" deemed="" as="" statistically="">

Abbreviazioni
AL: danno polmonare acuto; LPS: lipopolisaccaride; HMGB1: scatola di gruppo ad alta mobilità 1proteina; PPARy. Recettore gamma attivato dal proliferatore del perossisoma; MAPK: proteina chinasi attivata dal mitogeno; JNK: C-Jun NH(2)-chinasi terminale; CLP: legatura e puntura cecale; DMEM: mezzo Eagle modificato di Dulbecco; DMSO: dimetilsolfossido; CCK-8:kit per il conteggio delle cellule-8; LDH: lattato deidrogenasi; TUNEL: Etichettatura del nick-end mediata dalla deossinucleotidil transferasi terminale; PBS: tampone fosfato salino; DAB: diamminobenzene; AO/EB: Arancio di acridina/bromuro di etidio; BCA: acido bicinconinico; SDS-PAGE: elettroforesi su gel di sodio dodecil solfato-poliacrilammide; PVDF: polivinilidene difluoruro; ECL: chemiluminescenza potenziata; cDNA: DNA complementare; ELSA: test di immunoassorbimento enzimatico; IL: Interleuchina; TNF-a: fattore di necrosi tumorale-a; MDA: malondialdeide; GSH-Px Glutatione perossidasi; SOD: Superossido dismutasi; SD: deviazione standard; ANOVA: Analisi della varianza; Cox-2:ciclossigenasi-2; Nrf2: fattore nucleare eritroide 2-fattore correlato 2; ROS: specie reattive dell'ossigeno.
Riferimenti
1. Mokra D, Kosutova P. Biomarcatori nel danno polmonare acuto. Respir Physiol Neurobiol. 2015;209:52–8.
2. Hayes M, Curley G, Ansari B, Laffey JG. Revisione clinica: terapie con cellule staminali per danno polmonare acuto/sindrome da distress respiratorio acuto: speranza o clamore? Critico Cura. 2012;16(2):205.
3. Angus DC, Clermont G, Linde-Zwirble WT, Musthafa AA, Dremsizov TT, Lidicker J, et al. Costi sanitari e risultati a lungo termine dopo la sindrome da distress respiratorio acuto: uno studio di fase III sull'ossido nitrico per via inalatoria. Crit Care Med. 2006;34(12):2883–90.
4. Hu JT, Lai J, Zhou W, Chen XF, Zhang C, Pan YP, et al. L'ipotermia ha alleviato il danno polmonare acuto indotto da LPS nei modelli di ratto attraverso il percorso TLR2/MyD88. Ris. Polmone Esp. 2018;44(8–9):397–404.
5. Chi YS, Lim H, Park H, Kim HP. Effetti della wogonin, un flavone vegetale di Scutellaria radix, sull'infiammazione cutanea: regolazione in vivo dell'espressione genica associata all'infiammazione. Biochimica Farmaco. 2003;66(7):1271–8.
6. Wei CY, Sun HL, Yang ML, Yang CP, Chen LY, Li YC, et al. Effetto protettivo della wogonin sul danno polmonare acuto indotto da endotossina attraverso la riduzione della fosforilazione di p38 MAPK e JNK. Tossico ambientale. 2017;32(2):397–403.
7. Yeh YC, Yang CP, Lee SS, Horng CT, Chen HY, Cho TH, et al. Il danno polmonare acuto indotto dal lipopolisaccaride è inibito dalla wogonin nei topi attraverso la riduzione della fosforilazione di Akt e dell'attivazione di RhoA. J Pharm Pharmacol.2016;68(2):257–63.
