Un modello di ottimizzazione basato sulla simulazione per studiare l'impatto dell'elenco di più regioni e della condivisione delle informazioni sui risultati del trapianto renale
Mar 18, 2022
Zahra Gharibi 1,* e Michael Hahsler 2
Astratto:Più di 8000 pazienti in lista d'attesa perrenetrapianto muoiono o diventano non idonei a ricevere trapianti a causa del deterioramento della salute. Allo stesso tempo, più di 4000 reni recuperati da donatori deceduti vengono scartati ogni anno negli Stati Uniti. Questo documento sviluppa un modello di ottimizzazione basato sulla simulazione che considera diversi fattori cruciali per arenetrapianto per migliorarereneutilizzazione. A differenza della maggior parte dei modelli proposti, il modello di ottimizzazione presentato incorpora i dettagli del processo di offerta, il deterioramento della salute del paziente erenequalità nel tempo, la correlazione tra la salute dei pazienti e le decisioni di accettazione e la probabilità di accettazione del rene. Stimiamo i parametri del modello utilizzando i dati ottenuti dalla United Network of organ sharing (UNOS) e dal Scientific Registry of Transplant Recipients (SRTR). Utilizzando questi parametri, illustriamo la potenza del modello di ottimizzazione basato sulla simulazione utilizzando due applicazioni correlate. Il primo esplora gli effetti dell'incoraggiare i pazienti a perseguire liste d'attesa in più regioni sugli esiti post-trapianto. In questo caso, un modello di ottimizzazione basato sulla simulazione consente al paziente di selezionare le regioni migliori in cui essere inserito in lista d'attesa, dati i rapporti tra domanda e offerta. La seconda applicazione si concentra su un aspetto del trapianto a livello di sistema, vale a dire il contributo della condivisione delle informazioni sul miglioramento dei tassi di rigetto dei reni e del benessere sociale. Indaghiamo gli effetti dell'utilizzo della moderna tecnologia dell'informazione per accelerare la ricerca di un paziente corrispondente a un organo donatore disponibile sulla mortalità in lista d'attesa, rigetto di reni e tassi di trapianto. Dimostriamo che il moderno supporto della tecnologia dell'informazione attualmente sviluppato dalla United Network for Organ Sharing (UNOS) è essenziale e può migliorare significativamente l'utilizzo dei reni.
Parole chiave:modello di simulazione;reneaccettazione;reneassegnazione; elenco di più regioni; condivisione delle informazioni
Contatto:joanna.jia@wecistanche.com

Cistanchetubulosa previene le malattie renali, clicca qui per ottenere il campione
1. Introduzione
Cronicorenemalattia (CKD) è una progressiva perdita direnefunzione nel tempo. L'insufficienza renale cronica è una crisi sanitaria mondiale poiché, al momento, più di 2 milioni di pazienti soffrono di malattia renale allo stadio terminale (ESRD) o insufficienza renale. Si prevede che il numero di pazienti con diagnosi di ESRD aumenterà a un tasso compreso tra il 5% e il 7% ogni anno [1]. Al momento, non esiste una cura perrenefallimento e i pazienti con ESRD devono ricevere una dialisi frequente o un trapianto di rene da un donatore vivente o deceduto per sopravvivere. Per la maggior parte dei pazienti, il trapianto di rene è il trattamento preferito che fornisce un'aspettativa di vita più lunga con una qualità della vita superiore rispetto alla dialisi. Tuttavia, i pazienti di tutto il mondo si trovano ad affrontare una carenza cronica di reni di donatori accessibili per il trapianto.
Attualmente negli Stati Uniti, quasi 100,{1}} pazienti sono in lista d'attesa e, in media, vengono arruolati oltre 3000 nuovi pazienti ogni mese. Ogni anno, più di 4000 pazienti muoiono in attesa di un salvataggiorenetrapianto e oltre 4000 si ammalano troppo e si ammalano Per capire le ragioni dietro tassi di rigetti così elevati, dobbiamo guardare alreneprocesso di assegnazione e offerta. Esistono notevoli differenze tra i reni di donatori vivi e deceduti e tra i diversi paesi. Ci concentriamo qui surenida donatori deceduti negli Stati Uniti. I criteri più importanti per l'allocazione renale del donatore deceduto sono (1) compatibilità medica donatore-ricevente, (2) fattori logistici e (3) posizione del paziente nella lista d'attesa (p. es., tempo di attesa, punti). Più in particolare, negli Stati Uniti, la United Network of Organ Sharing (UNOS) amministra la Organ Procurement and Transpianation Network (OPTN) ed è responsabile della raccolta dei dati sia sui pazienti che sui donatori. Oltre alle informazioni logistiche e al tempo di attesa, i dati della lista d'attesa includono l'identità del paziente, i fattori demografici (p. es., sesso, razza, età) e le caratteristiche mediche (p. es., gruppo sanguigno ABO, antigeni leucocitari umani (HLA), panel reattivo anticorpo (PRA)). Allo stesso modo, per creare un database di donatori deceduti, UNOS ottiene informazioni sui dati demografici dei donatori, sulla logistica del donatore, sul recupero e sulla conservazione e sulle caratteristiche mediche del donatore. negli Stati Uniti sono stati trapiantati in totale 16.534 reni. Nonostante l'elevata domanda e la significativa carenza di reni, circa un rene su cinque recuperato da donatori deceduti viene scartato [2].
Per comprendere le ragioni alla base di tassi di rigetti così elevati, dobbiamo esaminare ilreneprocesso di assegnazione e offerta. Esistono notevoli differenze tra donatore vivente e donatore decedutorenie tra paesi diversi. Ci concentriamo qui sui reni di donatori deceduti negli Stati Uniti. I criteri più importanti per l'allocazione renale del donatore deceduto sono (1) compatibilità medica donatore-ricevente, (2) fattori logistici e (3) posizione del paziente nella lista d'attesa (p. es., tempo di attesa, punti). Più in particolare, negli Stati Uniti, la United Network of Organ Sharing (UNOS) amministra la Organ Procurement and Transpianation Network (OPTN) ed è responsabile della raccolta dei dati sia sui pazienti che sui donatori. Oltre alle informazioni logistiche e al tempo di attesa, i dati della lista d'attesa includono l'identità del paziente, i fattori demografici (p. es., sesso, razza, età) e le caratteristiche mediche (p. es., gruppo sanguigno ABO, antigeni leucocitari umani (HLA), panel reattivo anticorpo (PRA)). Allo stesso modo, per creare un database di donatori deceduti, UNOS ottiene informazioni sui dati demografici dei donatori, sulla logistica del donatore, sul recupero e sulla conservazione e sulle caratteristiche mediche del donatore.
UNOS utilizza una rete di computer centralizzata per collegare tutte le organizzazioni di approvvigionamento di organi (OPO) e centri trapianti. Per destinare donatoreni, UNOS utilizza il suo sistema di corrispondenza donatore-ricevente. Ogni volta un nuovo donatore decedutoreneviene recuperato per il trapianto, UNOS applica un algoritmo match-run, un programma che confronta i dati dei donatori con i dati dei pazienti in lista d'attesa attivi. Viene generato un elenco di pazienti in ordine di rango utilizzando le regole e le politiche di allocazione dei reni. I fattori considerati nella creazione di questo elenco includono il tempo di attesa, la compatibilità del sistema immunitario donatore-ricevente, l'idoneità alla priorità del donatore vivente, la distanza dall'ospedale del donatore, il beneficio di sopravvivenza (corrispondenza di longevità donatore-ricevente) e lo stato pediatrico.
Il processo di offerta completo è complesso e qui ci concentriamo solo sui componenti principali necessari per il modello di simulazione discusso in questo documento. Il processo inizia con i pazienti elencati nelle OPO locali (ci sono 58 OPO negli Stati Uniti, ciascuna con la propria area di servizio designata), che sono compatibili con il medico e hanno la massima priorità nella lista d'attesa. Se l'assegnazione locale non va a buon fine, l'organo viene offerto nella regione (gli Stati Uniti sono attualmente divisi in 11 regioni di trapianto) e infine a livello nazionale. Le figure 1a,b mostrano rispettivamente 11 regioni geografiche negli Stati Uniti [3] e la gerarchia geografica del processo di offerta del rene. Maggiori dettagli sull'approvvigionamento degli organi e sulla politica di assegnazione sono disponibili in [4]. Uno dei motivi per dare priorità ai pazienti locali nelreneprocesso di assegnazione è quello di ridurre il tempo tra il prelievo degli organi e l'impianto. Questo tempo è chiamato Cold Ischemia Time (CIT) e svolge un ruolo essenziale negli esiti del trapianto di rene [5,6].
La Figura 2 e la Tabella 1 mostrano le variazioni regionali in CIT, tempo di attesa ereneesiti del trapianto negli Stati Uniti, rispettivamente. C'è una variazione sostanziale nei tempi di attesa del rene del donatore deceduto negli Stati Uniti. Diversi fattori possono influenzare il tempo di attesa di un paziente fino al trapianto. Oltre ai fattori clinici del paziente come il gruppo sanguigno e il grado di sensibilizzazione mostrati dal PRA (anticorpo reattivo del pannello), la geografia e il luogo di residenza del paziente hanno un enorme effetto sulla possibilità di accedere a un trapianto di rene tempestivo. Questo è importante poiché le regioni con CIT più lunghe hanno maggiori probabilità di avere tassi di sopravvivenza dei pazienti e di trapianto post-trapianto inferiori. Più precisamente, come suggeriscono i risultati dei tassi di sopravvivenza del paziente e del trapianto a uno e cinque anni dopo un trapianto di rene, la regione 9 con il CIT più lungo tra tutte le regioni ha il tasso di sopravvivenza del paziente e del trapianto più basso tra tutte le 11 regioni. In genere, quando la CIT raggiunge le 24 h, è difficile trovare un paziente che accetti l'organo offerto. Nella maggior parte dei casi, i reni vengono scartati dopo 48 h di CIT. Pertanto, la riduzione della CIT renale attraverso miglioramenti gestionali potrebbe essere un modo conveniente per migliorare l'attuale sistema di trapianto e i risultati.
![Figure 1. (a) 11 geographic regions in the US [3], (b) Geographical hierarchy of kidney offering process. Figure 1. (a) 11 geographic regions in the US [3], (b) Geographical hierarchy of kidney offering process.](/Content/uploads/2022842169/2022011213442069f23e3bf4c24321bedec383620cde7b.png)


I chirurghi e le autorità di regolamentazione dei trapianti negli Stati Uniti hanno espresso le loro preoccupazioni per quanto riguarda l'alto osservatorenetassi di eliminazione nonostante la lista d'attesa in crescita, i lunghi tempi di attesa e l'alto tasso di rimozione della lista d'attesa. La tabella 2 mostra la lista d'attesa e le informazioni sui trapianti per gli Stati Uniti e per i paesi Eurotransplant (ET). Eurotransplant è un'organizzazione internazionale senza scopo di lucro responsabile dell'assegnazione e del trapianto di organi in Austria (A), Belgio (B), Croazia (HR), Germania (D), Ungheria (H), Lussemburgo (LR), Paesi Bassi (NL) e Slovenia (SLO). Anche se il numero di donatirenie i trapianti eseguiti nel 2019 negli Stati Uniti hanno raggiunto il massimo storico, il tasso di rigetto di rene di circa il 26% (calcolato come il numero di trapianti di rene deceduti oltre il doppio del numero totale di donatori deceduti) resta preoccupante, rispetto all'ET tasso di scarto dei paesi del 20 per cento.

Il motivo più comune per il donatorereneil rifiuto e il potenziale rigetto sono preoccupazioni per la qualità del rene del donatore. I dati mostrano che i chirurghi trapiantisti rifiuterebbero reni di bassa qualità per un paziente relativamente sano nella speranza di ricevere un'offerta migliore in futuro [7]. In aggiunta arenequalità,renei tassi di accettazione e di rigetto possono anche essere influenzati dal processo di assegnazione stesso [8]. L'evidenza mostra che i reni rifiutati all'inizio del processo di assegnazione hanno meno probabilità di essere accettati in seguito [9]. Un'altra preoccupazione è la crescente avversione al rischio dei centri trapianti a causa dei rapporti specifici del programma che valutano i risultati post-trapianto. Questi possono fornire incentivi ai centri per richiedere reni di qualità superiore. Di conseguenza, potrebbero rifiutare reni adeguati per il paziente, ma ciò comporta il rischio di avere un impatto negativo sulla valutazione dei loro risultati post-trapianto [8,10-15].
Un altro motivo per non osservare sufficientemente in altorenel'utilizzo è la disparità geografica degli Stati Uniti nell'accesso ai trapianti di rene. La tabella 3 mostra le disparità geografiche nel numero di donatori, OPO e centri trapianti deceduti nelle 11 regioni. Diversi stati come Wyoming, Idaho e Montana non hanno centri di trapianto nonostante il loro alto tasso di donazione di organi. Una tale variazione e differenza nelle OPO e nelle strutture per il trapianto di organi può portare a una disponibilità ingiusta degli organi, a uno scarso accesso alle cure e a lunghi tempi di attesa non necessari per alcuni pazienti. Uno dei cinque obiettivi strategici dell'UNOS è fornire equità nell'accesso ai trapianti e ridurre la disparità geografica [16]. Per aumentare le possibilità di ricevere un organo donato ben abbinato e ridurre i lunghi tempi di attesa, i pazienti possono spostarsi in una regione con tempi di attesa più brevi o arruolarsi in più centri di trapianto, tipicamente situati in regioni diverse [17]. L'UNOS ha stabilito più politiche di elenco che consentono ai pazienti di essere arruolati in più di un centro trapianti.

Attualmente, circa il 4% dei pazienti in attesa di arenei trapianti sono elencati in più elenchi, che è il tasso più alto tra tutti gli organi [18].
Come per qualsiasi arruolamento di trapianto, il paziente deve completare i test di valutazione e impegnarsi nel regolamento del centro trapianti, come la possibilità di raggiungere il centro trapianti entro un determinato tempo. Per l'arruolamento in più centri, questo processo può essere piuttosto costoso poiché la maggior parte delle compagnie assicurative potrebbe non rimborsare il costo di valutazioni aggiuntive [15,19]. Inoltre, i pazienti che ricevono trapianti di organi devono assumere farmaci immunosoppressori come parte delle cure post-trapianto per assicurarsi che il loro corpo non rigetti un nuovo organo [20]. Pertanto, un paziente deve sapere se l'assistenza post-trapianto può essere trasferita in un centro più vicino alla sua residenza. Senza politiche per un adeguato sostegno finanziario per le spese di viaggio, questo chiaramente pone ancora un problema in termini di equità ed equità che i responsabili politici devono affrontare.
In questo documento, introduciamo un modello di simulazione stocastica che può essere utilizzato per analizzare l'effetto delle modifiche al sistema di allocazione renale e al processo di offerta. Il modello di simulazione coinvolge la salute del paziente, la qualità del donatore-rene rappresentata daReneIndice del profilo del donatore (KDPI) [21], deterioramento della qualità del rene del donatore dovuto all'accumulo di CIT durante il processo di assegnazione, e anche domanda e offerta di rene. Inoltre, il modello considera la possibilità che un rene donatore non possa essere accettato per altri motivi (es. malattia a breve termine del paziente, risorse chirurgiche insufficienti, risultato di cross-matching). Utilizzando i parametri del modello stimati dai dati forniti da UNOS e dal Registro Scientifico dei Destinatari del Trapianto (SRTR), applichiamo il modello di simulazione per studiare le seguenti due tendenze cruciali per migliorare i tassi di trapianto di rene da donatore:
Lista multipla: il trasferimento in una regione con un tempo di attesa più breve o la lista d'attesa in più regioni può aiutare un paziente aumentando le sue possibilità di ricevere un trapianto di rene prima. Di conseguenza, il paziente può migliorare i risultati post-trapianto a causa del minor deterioramento della salute dovuto alla permanenza in dialisi. Tuttavia, lo sviluppo di una strategia per guidare la decisione del paziente di trasferire o multi-listing non è facile. Formuliamo la decisione come un problema di massimizzazione dell'utilità in una serie di vincoli di budget, distanza e struttura a livello regionale. L'offerta e la domanda variano ampiamente nelle 11 regioni degli Stati Uniti e per i diversi gruppi sanguigni. Tale variazione si traduce in tempi di attesa ampiamente variabili, che portano a diverse utilità attese e strategie di accettazione renale ottimali (espresse come soglie di qualità renale ottimale). Per derivare l'utilità di un paziente per diverse regioni, utilizziamo il modello di simulazione per ottenere l'utilità in base a decisioni di accettazione del trapianto di rene ottimali individualizzate in base allo stato di salute del paziente e all'offerta e alla domanda del gruppo sanguigno del paziente. Usiamo le informazioni ottenute per risolvere il problema di ottimizzazione e derivare una politica di selezione della regione ottimale.
Tecnologia dell'informazione: una comunicazione rapida e precisa tra UNOS e centri trapianti è necessaria per rendere più efficiente l'allocazione degli organi, che diventa persino più critica di fronte ai pazienti multi-elencati. L'UNOS ha l'obiettivo di aumentare l'uso della tecnologia dell'informazione nell'allocazione e nel trapianto di organi. Hanno implementato un sistema online sicuro che raccoglie dati per migliorare la capacità del sistema di trapianto di aumentare le possibilità del paziente di ricevere un organo salvavita. Con l'evoluzione della tecnologia, UNOS incoraggia anche lo sviluppo e l'utilizzo di tecnologie moderne come i dispositivi mobili per una considerazione più rapida ed efficiente dei donatorireneoffre di ottenere un tasso di utilizzo dei reni più elevato [22]. Ad esempio, i dispositivi mobili renderanno più facile raccogliere la disponibilità aggiornata dei pazienti per il trapianto (ad esempio, tramite un'app). Utilizzando queste informazioni, OPTN assegnerà il rene più velocemente, riducendo il deterioramento del rene e lo scarto. Nel caso ideale di perfetta informazione, OPTN potrebbe trovare il primo paziente in lista d'attesa che accetterà immediatamente ilrene, riducendo CIT e scartare al minimo. La simulazione presentata valuta l'effetto di un caso realistico di condivisione delle informazioni imperfetta.
2. Revisione della letteratura
In questa sezione, esaminiamo gli studi medici e analitici sul trapianto di organi rilevanti per questo articolo. Per i documenti medici, ci concentriamo principalmente sulla CIT e sull'attesa della dialisi come due fattori di rischio indipendenti gestibili che contribuiscono efficacemente ai risultati del trapianto renale. Per la sezione analitica, esaminiamo i documenti che rientrano in uno o entrambi i due flussi di ricerca relativi al processo decisionale per accettare gli organi del donatore deceduto e alla progettazione del processo di assegnazione.
2.1. Letteratura medica
Diversi ricercatori in Nord America, Sud America ed Europa hanno studiato l'associazione tra CIT ereneesiti del trapianto [23,24]. L'analisi fatta da Nieto-Ríos et al. [25] mostra che la CIT è un fattore di rischio indipendente per la funzione del trapianto ritardato (DGF). Più precisamente, il rischio di sviluppare DGF aumenta quando CIT supera le 18 h. Tuttavia, non ha un impatto negativo sui risultati del rigetto acuto o della perdita dell'innesto post-trapianto a un anno.
Uno studio francese di Debout et al. [26] rileva che il rischio di fallimento e mortalità dell'allotrapianto post-trapianto aumenta notevolmente per ogni ora aggiuntiva di CIT. Uno studio simile condotto da Valdivia et al. [27] in Andalusia, Spagna, conferma che una CIT prolungata può avere un impatto sui tassi di sopravvivenza sia del paziente che del trapianto. Lo studio suggerisce che la CIT lunga può aumentare il rischio di una scarsa funzionalità iniziale dell'innesto indipendentemente dall'età del donatore e del ricevente. Con l'aumento del CIT, aumenta anche la possibilità di DGF. Tuttavia, l'associazione dannosa di CIT prolungata con il rischio di DGF non è amplificata nei donatori più anziani (p. es., criteri estesi, donatori). Lo studio mostra che l'effetto della CIT sul rigetto acuto del trapianto renale (ARTR) è più evidente tra i pazienti sottopostireneritrapianto. L'analisi suggerisce inoltre che i reni donati con una CIT di 24 h o più sono a maggior rischio di ARTR rispetto a quelli di organi con CIT inferiore a 12 h. Koizumi et al. [6] riportano che negli Stati Uniti sono state osservate variazioni regionali negli esiti renali, ma il motivo principale alla base di queste variazioni non è chiaro. Lo studio rivela significative variazioni del tempo di ischemia fredda (CIT) tra le regioni per i reni dei donatori. In particolare, trovano che le regioni con CIT più lunga hanno maggiori probabilità di avere un tasso di sopravvivenza renale post-trapianto inferiore. Suggeriscono che i miglioramenti gestionali possono essere una scelta economicamente vantaggiosa per migliorare le prestazioni del sistema di trapianto attuale e la potenzialità di ridurre i tassi di rigetto degli organi.
Meier-Kriesche et al. [28] utilizzano i dati del Renal Data System Registry (USRDS) degli Stati Uniti per considerare la potenziale associazione tra il tempo di attesa e gli esiti del trapianto renale. Il loro studio conferma che i lunghi tempi di attesa sono un fattore di rischio significativo che influisce negativamente sui benefici della sopravvivenza del trapianto renale. Di conseguenza, suggeriscono che prima i pazienti con ESRD ricevono un trapianto renale, maggiori sono le loro possibilità di sopravvivenza a lungo termine. Meier-Kriesche e Kaplan [29] studiano l'importanza del tempo di attesa durante la dialisi come il più sostanziale fattore di rischio indipendente sureneesiti del trapianto. Come parte della loro analisi, applicano le stime di Kaplan-Meier e i modelli dei rischi proporzionali di Cox al database del sistema di dati renali degli Stati Uniti per esplorare l'effetto del tempo di attesa sul donatore decedutorenerisultati. I loro risultati mostrano che i tassi di sopravvivenza del trapianto a cinque e dieci anni sono significativamente peggiori tra i riceventi di rene accoppiati che hanno aspettato per più di due anni in dialisi rispetto ai pazienti accoppiati.renedestinatari con un tempo di attesa inferiore a sei mesi.
2.2. Letteratura Analitica
La letteratura analitica si concentra sulla progettazione delreneprocesso di allocazione e utilizza spesso modelli di simulazione. Le questioni discusse sono l'efficacia e l'equità del processo di assegnazione e l'effetto della decisione di accettazione del rene.
Per analizzare il processo di allocazione utilizzato nel 2000, Zenios et al. [30] propongono un'allocazione dinamica delle risorse che massimizza l'aspettativa di vita del paziente dal ricevere un trapianto di rene riducendo al minimo l'iniquità tra i pazienti. Il modello di simulazione costruito mostra che la politica di assegnazione degli organi attualmente utilizzata aumenta l'aspettativa di vita adeguata alla qualità del paziente e riduce il tempo di attesa previsto.
Ilrenedecisione di accettazione è centrale per un intero flusso di ricerca. Ahn e Hornberger [31] sviluppano un modello teorico che considera la salute del paziente nel prendere una decisione di accettazione/rifiuto riguardante la qualità dei reni offerti. La loro analisi rivela che un paziente relativamente sano può permettersi di essere selettivo sulla qualità di un donatorerenie si aspettano di ricevere un migliore risultato post-trapianto accettando un rene di alta qualità. L'effetto della scelta del paziente sul sistema di allocazione degli organi è studiato da Su e Zenios [32]. Lo studio introduce un modello di accodamento che analizza gli effetti della scelta del paziente sui tassi di rigetto renale valutando le prestazioni del sistema di attesa in base alle politiche first-com-first-serve (FCFS) e last-come-first-serve (LCFS). Concludono che LCFS è più efficiente di FCFS. Infatti, contrariamente a LCFS, la politica FCFS incentiva i pazienti a rifiutare reni di bassa qualità, con conseguente basso utilizzo dei reni. D'altra parte, il modello mostra che la politica LCFS ottiene un utilizzo ottimale degli organi. In uno studio diverso, Su e Zenios [33] studiano il ruolo della scelta del paziente nell'allocazione renale utilizzando un modello di assegnazione stocastica sequenziale. Il modello affronta il conflitto tra scelta del paziente e benessere sociale. L'analisi considera due schemi, in cui il primo presuppone che i pazienti debbano accettare qualsiasi rene offerto. La prima soluzione migliore è trovare una politica di allocazione che massimizzi il benessere sociale. Introducendo la scelta del paziente, la politica del primo migliore viene modificata per ottenere una politica del secondo migliore. Di conseguenza, viene introdotta una condizione di compatibilità degli incentivi, che costringe la politica di assegnazione a essere progettata in modo tale da garantire che i pazienti accettino qualsiasi offerta renale. Su e Zenios [34] introducono un modello di progettazione del meccanismo per l'allocazione degli organi che tiene conto della scelta del paziente. I pazienti dichiarano i tipi di rene (p. es., la qualità) che desiderano ricevere quando si uniscono alla lista d'attesa per il trapianto di rene (non al momento dell'offerta di rene del donatore) e si uniscono alla coda che serve il tipo di rene dichiarato. In questo modo, il modello riduce il lungo processo di ricerca identificando i pazienti appropriati che desiderano accettare più efficacemente i reni di donatori recuperati.
L'equità e l'equità sono argomenti importanti Bertsimas et al. [35] studiano le disparità geografiche nell'accesso al donatore decedutoreni. Usano un'approssimazione fluida per un modello di coda per formulare il modo ottimale per l'arruolamento di un paziente nelle liste di attesa di più centri trapianti. L'obiettivo del paziente è massimizzare l'aspettativa di vita riducendo al minimo il costo della congestione. Combinando risultati analitici, di simulazione e numerici, mostrano che l'elenco multiplo promuove notevolmente l'equità geografica e aumenta il donatorerenela fornitura. Avere più donatori porta a un tasso di trapianto più elevato e riduce il tasso di mortalità dei pazienti in lista d'attesa. Alcuni studi [36-38] hanno sviluppato modelli che consentono a una coppia incompatibile di donatore-ricevente ancora di ricevere un rene donatore vivente tramite uno scambio con altre coppie incompatibili donatore-ricevente. Sebbene la maggior parte dei modelli esistenti miri a massimizzare il numero totale di possibili scambi renali e benessere sociale, non considerano la componente di equità definita come soddisfazione del donatore-ricevente. Lee et al. [39] presentano un modello di programmazione stocastica a due stadi che considera l'equità nei programmi di scambio renale di donatori viventi. Lo studio esamina molteplici scenari per studiare l'effetto dell'equità sugli esiti dello scambio renale. I risultati numerici mostrano il miglioramento dell'esito del programma di scambio di donatori viventi quando si tiene conto dell'equità nell'abbinamento di coppie incompatibili. Si noti che alcuni studi discussi qui considerano l'impatto dell'equità nel trapianto di rene vivente; tuttavia, ci concentriamo solo sui trapianti utilizzando reni di donatori deceduti.
Le simulazioni presentate in letteratura utilizzano ipotesi forti. Ad esempio, Su e Zenios [33] presumono che i pazienti debbano accettare qualsiasi offertarene, o in [34] i pazienti non possono modificare la qualità renale scelta inizialmente. Inoltre, la maggior parte delle simulazioni si concentra in genere su una singola variabile. Ad esempio, lo studio di Ruth et al. [40] si concentra sulla lunghezza della lista d'attesa. Lo studio propone un modello di simulazione per il processo di assegnazione degli organi e rileva che nelle condizioni di assegnazione degli organi nel 1985, la lunghezza della lista d'attesa continuerà a crescere. Il modello di simulazione che presentiamo in questo documento fornisce un quadro più completo considerando l'effetto delle decisioni del paziente, dell'offerta e della domanda in diverse regioni, l'efficienza del processo di allocazione e l'effetto atteso dell'utilità post-trapianto.

bodybuilding per le lunghe
3. Descrizione dei modelli
Nelle sezioni seguenti, discutiamo in dettaglio i componenti principali sia dei modelli di simulazione che di ottimizzazione. I modelli di simulazione includono paziente (domanda d'organo), donatore decedutoreniarrivo (fornitura di organi), il processo di offerta consecutiva di rene del donatore deceduto per trovare la soglia di qualità renale ottimale e l'utilità post-trapianto prevista per un paziente con un determinato livello di salute. Utilizziamo quindi l'output del modello di simulazione come coefficienti della funzione obiettivo del modello di ottimizzazione per raccomandare una politica di elenchi multipli e suggeriamo un insieme di regioni che il paziente può scegliere.
3.1. Modello di simulazione
Sviluppiamo un modello di simulazione che consente al paziente di identificare l'ottimalerenesoglia di qualità che massimizza la sua utilità post-trapianto. I parametri del modello dipendono dall'offerta e dalla domanda della regione dei pazienti. Simuliamo ilrenestrategia di accettazione e l'utilità post-trapianto risultante corrispondente a ciascun trapianto. La figura 3 illustra il processo di simulazione. Discutiamo i componenti chiave nelle sezioni seguenti.

3.1.1. Domanda d'organo
La domanda è rappresentata dai pazienti in lista d'attesa. Abbiamo suddiviso i pazienti in diversi gruppi di pazienti competitivi che possono ricevere lo stesso tipo di organo donatore deceduto a seconda dei gruppi sanguigni e di altri criteri clinici. Modelliamo ogni gruppo separatamente. Prenderemo in considerazione l'interazione tra i gruppi (p. es., alcuni pazienti con gruppo sanguigno AB possono ricevere organi da donatori con qualsiasi gruppo sanguigno) regolando l'apporto di organi ai singoli gruppi.
Ciascun gruppo di pazienti competitivo è modellato da una coda relativa al gruppo sanguigno j dove j ∈ {A, B, AB, O}. I pazienti possono unirsi alla loro coda abbinata (p. es., in base al gruppo sanguigno) con il tasso di λj ed essere serviti da donatori compatibili. Compatibilereniarrivare alla coda del gruppo sanguigno j con una frequenza di µi. Ad esempio, per la coda di gruppo sanguigno A, compatibilerenisono di tipo A e O. I pazienti escono dalla lista d'attesa j con un tasso di trapianto di ηi quando (1) accettano un rene offerto, o (2) con un tasso di θi si ammalano troppo per il trapianto o muoiono in lista d'attesa . La struttura del modello di accodamento è mostrata nella Figura 4.
A seguito dello studio in [34], i pazienti di gruppo sanguigno j arrivano secondo un processo di Poisson con il tasso di arrivo di λj per unirsi alla lista d'attesa. I pazienti si uniscono alla lista di attesa nel modello con uno stato di salute iniziale non osservabile h0 che rappresenta il tempo rimanente in cui possono sopravvivere alla dialisi quando si uniscono. Modelliamo la distribuzione di h0 nella popolazione di pazienti utilizzando una distribuzione Weibull. La distribuzione di Weibull viene spesso utilizzata nell'analisi di sopravvivenza per rappresentare il tempo al fallimento poiché è in grado di esprimere tassi di fallimento decrescenti, costanti o in aumento nel tempo. La salute di un paziente simulato, h0, è quindi la realizzazione di una variabile casuale H0 ∼ Weibull(a, b), dove a e b sono rispettivamente i parametri di scala e di forma. I pazienti escono dalla lista d'attesa se (1) ricevono un trapianto o (2) lasciano la coda a causa di cattive condizioni di salute (o morte). Poiché h0 è il tempo in cui il paziente può sopravvivere in dialisi quando si unisce alla lista d'attesa (cioè, l'indice indica che ha aspettato zero anni finora), la salute effettiva dopo aver aspettato w anni è hw {{1{{ 11}}}} h0 - w che significa che il paziente lascerà la lista d'attesa al più tardi quando w=h0.

3.1.2. Fornitura di organi
A seguito di [34], donatore deceduto compatibilereniarrivare alla coda per il gruppo sanguigno j secondo un processo di Poisson omogeneo indipendente con tasso di arrivo µj. OPTN definito arenemetrica di qualità chiamata Kidney Donor Profile Index (KDPI) che incorpora dieci fattori clinici del donatore per classificare i reni in base alla sopravvivenza renale stimata dopo il trapianto [41]. KDPI considera le seguenti caratteristiche del donatore: età, altezza, peso, etnia, se il donatore è morto a causa della perdita della funzione cardiaca o della funzione cerebrale, ictus come causa di morte, storia di ipertensione, storia di diabete, esposizione a il virus dell'epatite C, la creatinina sierica (una misura della funzionalità renale). Per costruzione, KDPI è quasi distribuito uniformemente su tutti i reni raccolti in un determinato anno. Seguendo KDPI, modelliamo la qualità di un rene donatore in arrivo mostrato con q0 come realizzazione di una variabile casuale Q ∼ Unif(0, 1). Usiamo 0 per rappresentare la qualità renale più bassa e 1 la più alta, cioè q0=1 - KDPI. Quando nella simulazione diventa disponibile un nuovo rene donatore, il rene viene simultaneamente offerto a un gruppo di pazienti g con una finestra temporale specificata per considerare l'offerta e prendere la decisione di accettazione/rifiuto. Se nessuno nel gruppo di pazienti g può accettare il rene dopo il tempo assegnato, il rene viene offerto al gruppo successivo di pazienti g in lista d'attesa. Il processo di assegnazione continua fino a quando l'organo non viene accettato da un paziente o scartato (a causa di una ricerca o di un posizionamento dell'organo non riusciti). Per l'attuale carenza di reni da donatori, abbiamo µj < λj,="" cioè="" i="" reni="" arrivano="" a="" un="" tasso="" inferiore="" rispetto="" ai="" nuovi="" pazienti.="" la="" rimozione="" del="" paziente="" per="" salute="" o="" morte="" mantiene="" la="" coda="" a="" una="" dimensione="" limitata.="" liste="" d'attesa="" più="" lunghe="" comportano="" tempi="" di="" attesa="" più="" lunghi="" e="" un="" maggiore="" deterioramento="" della="" salute="" dei="" pazienti.="" a="" sua="" volta,="" questo="" aumenta="" il="" tasso="" di="" rimozione="" (pazienti="" che="" lasciano="" senza="" ricevere="" un="" trapianto).="" la="" lunghezza="" della="" coda="" si="" stabilizza="" all'equilibrio="" in="" cui="" il="" tasso="" di="" trapianto="" più="" il="" tasso="" di="" rimozione="" del="" paziente="" corrispondono="" al="" tasso="" di="" arrivo="" del="">
3.1.3. Decisione di accettazione/rifiuto del rene
Nel tempo, come il processo del donatorerenel'offerta continua, il rene si accumula CIT e la sua qualità si deteriora. Modelliamo questo deterioramento come qt {{0}} f(q0, δ, t). In questa equazione, t rappresenta il CIT accumulato e q0 rappresenta la qualità del rene al momento del recupero quando t=0. La variabile δ rappresenta un fattore di deterioramento della qualità del rene. Si richiede che la funzione di qualità f sia decrescente in δ e t, cioè ∂ f(q0,δ,t)∂δ < 0="" e∂="" f="" (q0,δ,t)="" ∂t="">< 0.="" nel="" modello="" di="" simulazione,="" misuriamo="" il="" tempo="" come="" multipli="" del="" tempo="" concesso="" per="" un="" giro="" di="" offerte.="" se="" i="" pazienti="" hanno="" un'ora="" per="" decidere,="" allora="" t="" rappresenta="" la="" città="" accumulata="" in="" ore.="" modelliamo="" il="" rene="" accetta/rifiuta="" la="" decisione="" del="" paziente="" e="" il="" successivo="" trapianto="" in="" due="" fasi.="" in="" primo="" luogo,="" il="" paziente="" utilizza="" una="" strategia="" di="" soglia="" per="" decidere="" se="">reneè accettabile. Il paziente accetterebbe l'offerta se qt Maggiore o uguale a k, dove k è la soglia di qualità renale decisa dal paziente e dal chirurgo. Per reni accettabili, prendiamo in considerazione diversi fattori legati alla salute del paziente e al centro trapianti. Nel modello di simulazione, utilizziamo la probabilità che il trapianto venga eseguito dato che viene offerto un rene accettabile

dove p(fattori del paziente) rappresenta la situazione medica specifica del paziente e qualsiasi fatto che il paziente o il chirurgo possono decidere contro ilreneper ragioni non spiegate esclusivamente dalla qualità del rene (p. es., il paziente è temporaneamente inattivo in lista d'attesa, risultato sfavorevole di cross-matching). La probabilità p(fattori centrali) rappresenta la disponibilità del centro trapianti (ad es. disponibilità di personale, sale operatorie, ecc.) nonché considerazioni sull'impatto del trapianto sulla valutazione delle prestazioni del centro. Il paziente sceglie la sua soglia di decisione k in consultazione con il chirurgo. Tale soglia sarà influenzata dalla salute del paziente h0 poiché un paziente che ha più tempo a disposizione per la dialisi attenderà un rene di migliore qualità. Modelliamo questa relazione nella simulazione scegliendo per ogni paziente da una variabile casuale K ∼ Unif(0,1) che è correlata con il paziente sh0 rappresentato da un coefficiente di correlazione di rango di Spearman di ρH 0, K.
3.1.4. Utilità post-trapianto del paziente
Se il paziente accetta il donatore decedutorenesi verifica l'offerta e il trapianto, un paziente riceve un'utilità post-trapianto. L'utilità post-trapianto dipende dalla qualità del rene al momento del trapianto qt e dal tempo di attesa del paziente w che determina lo stato di salute di hw=h0 - w. L'utilità post-trapianto può essere suddivisa in due componenti

dove B(·) rappresenta il beneficio per il paziente a seconda delrenequalità e D(·) rappresenta il deterioramento del paziente in lista d'attesa. La suddivisione dell'utilità in queste due componenti offre vantaggi per la stima dei parametri dai dati. La funzione B(·) può essere vista come il beneficio per il paziente se ricevesse un rene con qualità qt senza aspettare. La funzione del beneficio deve soddisfare che aumenta con la salute del paziente h{{0}} e la qualità del rene, cioè ∂B(∂hh00, qt) > 0 e ∂ B(∂hq0t, qt) > 0. D(·) rappresenta un costo sotto forma di fattore di deterioramento dovuto all'attesa w per il rene. La funzione di costo deve aumentare all'aumentare e diminuire del tempo di attesa con la salute del paziente., cioè Un modo comune per definire funzioni come B(·) è nella forma di regressione logistica per la sopravvivenza proposta da Cox [42] che modella le probabilità condizionali di morire in qualsiasi momento dato la sopravvivenza fino a quel momento

dove m(h{{0}}) indica l'esito del trapianto per un paziente con livello di salute h0 che ha ricevuto subito un rene perfetto (qt=1) (w {{3 }}). Naturalmente, m(h0) aumenta con la salute del paziente h0. Usiamo per D(·) il funzionale da

dove controlla il tasso di deterioramento. Il fattore di deterioramento è uguale a uno (cioè nessun deterioramento) quando il tempo di attesa è zero (w {{0}}). Se il paziente attende un rene di qualità molto elevata ed esaurisce il tempo (cioè, w=h0), il fattore di deterioramento diventa zero. La forma funzionale scelta è molto flessibile e può esprimere un deterioramento lineare ( {{ 4}}), rallentando il deterioramento ( > 1) e aumentando il deterioramento ( < 1).="" stimando="" i="" parametri="" dai="" dati="" e="" utilizzando="" l'ottimizzazione="" della="" simulazione,="" possiamo="" trovare="" per="" ogni="" paziente="">renesoglia di qualità k∗che massimizza l'utilità post-trapianto.
3.2. Selezione della regione e modello di ottimizzazione di elenchi multipli
Un paziente può aumentare le sue possibilità di ricevere un trapianto trasferendosi in una regione diversa (selezione della regione) o inserendosi in centri trapianti in più regioni. Per aiutare il paziente a identificare un insieme di regioni per l'arruolamento multiplo, utilizziamo il modello di simulazione per calcolare il parametro di soglia ottimale k∗i e l'utilità massima attesa che è probabile che un paziente ottenga da un trapianto in ciascuna regione. Questo è rappresentato da 11 valori di utilità Ui(k∗i , h0, w), i ∈ 1, 2, . . . , 11. Per semplicità, scriviamo Ui(k∗i ) per rappresentare l'utilità attesa post-trapianto per un paziente con date h0 e w. La selezione della regione viene ora eseguita selezionando la regione con l'utilità più grande.
Per l'elenco multiplo, rappresentiamo l'azione dell'arruolamento nella regione i mediante la variabile di decisione binaria

Il paziente ha 11 variabili decisionali, una per ciascuna regione. Assumiamo che la paziente vorrà aumentare le sue possibilità elencando le migliori regioni con la più alta utilità attesa data una serie di vincoli. Questo può essere formulato come il seguente problema di ottimizzazione.

Sommando l'utilità della regione si assicura che le regioni con le utenze maggiori siano incluse nella soluzione. Il primo vincolo assicura che la soluzione soddisfi il budget totale C del paziente dato. Il secondo vincolo considera la distanza massima che il paziente può percorrere per arrivare in tempo al centro trapianti. Il terzo vincolo considera le aspettative del paziente sulle prestazioni P della regione e, infine, l'ultimo vincolo limita rito a 0 o 1. Poiché il numero di regioni è piccolo, con solo 11, questo problema può essere risolto mediante l'enumerazione.
4. Applicazioni e risultati numerici
Iniziamo questa sezione stimando i parametri necessari per il modello di simulazione e quindi presentiamo come il modello può essere utilizzato per due applicazioni. La prima applicazione illustra come il modello può fornire una linea guida strategica per supportare la scelta del paziente di trasferirsi in una regione diversa o arruolarsi in più regioni.
La seconda applicazione analizza i potenziali vantaggi dell'utilizzo della moderna tecnologia delle informazioni condivise (ad es. tramite app per smartphone) per migliorare il benessere sociale aumentando l'utilità post-trapianto dei pazienti erenetassi di utilizzo.

bodybuilding per le lunghe
4.1. Stima dei parametri
Utilizziamo i dati di UNOS e SRTR per stimare i parametri del modello. Estraiamo UNOSdata per l'anno 2019 per stimare le aggiunte alla lista d'attesa e il donatorerenela fornitura. Per il calcolo del tempo di attesa, utilizziamo i valori riportati da SRTR. Il sistema di dati SRTR contiene dati medici e demografici dettagliati per tutti i donatori, i pazienti in lista d'attesa e i trapiantati negli Stati Uniti. Il set di dati utilizzato comprende più di 400,{1}} pazienti che hanno ricevuto per la prima volta un trapianto di rene da donatore deceduto tra ottobre 1987 e fine 2019.
I rapporti annuali di SRTR e UNOS forniscono informazioni sugli arrivi di organi e sull'attività in lista d'attesa (ad es. statistiche sull'aggiunta e l'espianto dei pazienti). Usiamo questi dati per stimare λj e µjin per ogni periodo.
Un fattore importante per stimare il tasso di arrivo del rene in una coda di gruppo sanguigno j è la compatibilità del gruppo sanguigno tra pazienti e donatori. Secondo i criteri di compatibilità del gruppo sanguigno, i donatori con gruppo sanguigno O sono donatori universali i cui organi renali possono essere offerti a pazienti di tutti i gruppi sanguigni. D'altra parte, i donatori con gruppo sanguigno AB possono donare i loro reni solo a pazienti di gruppo sanguigno AB mentre sono riceventi universali di tutti i gruppi sanguigni. La tabella 4 mostra in dettaglio la compatibilità del gruppo sanguigno per un trapianto di rene. Questo documento riporta solo i risultati per il gruppo sanguigno A. I risultati per altri gruppi sanguigni possono essere ottenuti in modo simile. La tabella 5 mostra i donatori e gli arrivi di pazienti per il gruppo sanguigno A.

Sulla base dei dati SRTR, i pazienti di gruppo sanguigno A ricevono in media il 94% e il 6% degli organi da donatori di gruppo sanguigno A e O, rispettivamente, il che si riflette nelreneparametro di fornitura µj nella Tabella 5. Seguendo l'attuale schema di offerta utilizzato da OPTN negli Stati Uniti, utilizziamo la dimensione del gruppo di pazienti di g=5 nel nostro modello di simulazione. Abbiamo impostato il tasso di degradazione renale δ al 5% secondo i rapporti secondo cui gli organi vengono usati raramente dopo un CIT di 48 ore [6]. A δ=0.05, la qualità del rene si deteriora a (1 − 0.05) {{10}}.5 percentuale della sua qualità iniziale dopo 48 h. Sulla base di discussioni con un collaboratore medico, utilizziamo una probabilità di trapianto p(trapianto)=0.8 per tutte le regioni. Una probabilità per ciascuna regione potrebbe anche essere stimata dai dati, ma al momento non ci sono disponibili informazioni sui rigetti delle offerte di reni. I parametri , , e per la funzione di beneficio B(h0, qt) e il fattore di costo C(h{{30}}, w) possono essere stimati se i dati di esito, compreso il post -è disponibile la sopravvivenza del trapianto. Tuttavia, poiché il nostro set di dati non include questi dati, nella nostra simulazione utilizziamo=0.4,=8 e=0.5. Aggiungiamo i pazienti alla lista d'attesa con un h0 di salute tratto da una variabile casuale H0 con una distribuzione Weibull. Utilizziamo un parametro di scala a=8 e un parametro di forma b=2 per ottenere una salute media di quasi 7 anni e circa il 90% della popolazione al di sotto dei 12 anni. Usiamo una correlazione di rango di Spearman ρ(H0, K) di 0,2, vicina alla correlazione tra la qualità del rene accettata e la salute del paziente osservata nei dati.

4.2. Selezione della regione ed elenco multiplo
Per illustrare l'approccio di selezione della regione, riportiamo i risultati per un paziente target con gruppo sanguigno A, un anno di vita in dialisi (h0=1) che è attualmente in posizione 100 della lista d'attesa. Soddisfiamo la lista d'attesa con pazienti generati casualmente (la cui salute è tratta da una distribuzione Weibull con una soglia politica correlata). Eseguiamo la stessa simulazione 100 volte ciascuna per i valori di soglia di decisione k ∈ {0, 0.1, 0.2, · · ·, 0.9} e media dei risultati delle 100 esecuzioni per stimare l'utilità attesa per ogni soglia.
La tabella 6 riporta i risultati per la soglia ottimale, k∗i , risultando nella più grande utilità post-trapianto attesa, Ui(k∗i ), per ciascuna regione. Ilreneil tasso di arrivo in coda (pazienti di tipo A in lista d'attesa) all'anno è µA e qt è la qualità media del rene trapiantato. Ad esempio, se il paziente target è arruolato nella regione 6, una soglia di k=0.65 è ottimale, il che porta a un'utilità di 9,6 anni. Al contrario, se è arruolata nella regione 2, la decisione ottimale può arrivare fino a 0.85 con un'utilità di 13,22 anni.
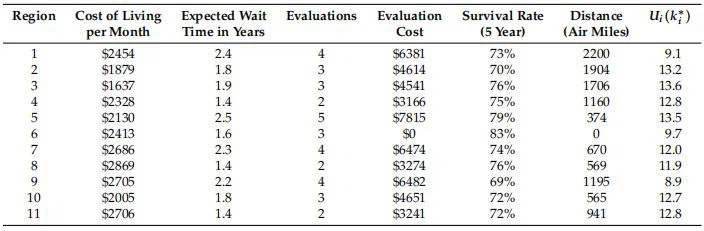
La tabella 7 rappresenta i dati stimati che abbiamo utilizzato nel nostro modello di ottimizzazione per trovare un insieme di regioni fattibili per un paziente di gruppo sanguigno A che si presume sia attualmente vivo e arruolato nella regione 6. Utilizziamo un set di dati UNOS per stimare il tempo di attesa previsto e il { {2}}tasso di sopravvivenza all'anno per tali pazienti in tutte le 11 regioni. In ogni regione, scegliamo una grande città e stimiamo il corrispondente costo della vita mensile utilizzando l'indice del costo della vita della città. Il costo di valutazione è definito come il prodotto del numero totale previsto di valutazioni fino arenetrapianto e il costo per valutazione. Il numero previsto di valutazioni è stimato sulla base di una politica di rivalutazione di 6-mese richiesta dalla maggior parte dei centri trapianti. In generale, la paziente è responsabile del pagamento del costo della valutazione periodica se desidera essere arruolata in più di una regione poiché la maggior parte delle polizze assicurative copre il costo della valutazione periodica di una sola iscrizione. Il costo totale è calcolato come segue: l'importo totale di denaro che un paziente deve pagare (numero di valutazioni per costo della valutazione) più il costo del viaggio e della permanenza in un'altra regione per tre giorni.
Ad esempio, qui assumiamo che il paziente abbia un budget di C=$ 15,000. Può anche viaggiare fino a D=1500 miglia e la sua aspettativa minima dalle prestazioni di una regione è del 75% della sopravvivenza a cinque anni. Con l'intenzione di massimizzare il suo risultato post-trapianto sotto questi tre vincoli, il nostro modello rileva che oltre alla regione di origine 6, la paziente può anche essere arruolata nelle regioni 5, 4 o 8, con la regione 5 che fornisce la massima utilità attesa. OPTN si impegna a fornire equità nell'accesso ai trapianti ea ridurre le disparità geografiche [16]. Con l'elenco multiplo gratuito, i pazienti hanno un incentivo a iscriversi a quante più regioni possibile, dati i loro vincoli di budget. Ciò significa che l'accesso al trapianto è influenzato dalle risorse finanziarie del paziente, il che può rappresentare un problema in termini di equità ed equità. Tuttavia, a lungo termine, la selezione gratuita della regione e gli elenchi multipli possono ridurre le disparità geografiche. Un numero maggiore di pazienti si arruola nelle regioni che attualmente offrono un'utilità maggiore, livellando le disparità di domanda e riducendo il divario di utilità. A quel punto, il vantaggio di avere più budget da arruolare in più regioni diminuirà, portando a una situazione più equa. A breve termine, l'equità deve essere temporaneamente assicurata da politiche appropriate per rendere disponibili più elenchi a più pazienti.

4.3. L'effetto della condivisione delle informazioni sull'efficienza dell'allocazione
Una delle iniziative del Piano Strategico OPTN (2018–2021) [16] con l'obiettivo di aumentare il numero di trapianti è quella di perseguire strumenti di sistema per un abbinamento donatore/ricevente più efficiente. Tali strumenti includono strumenti per la condivisione delle informazioni, il che significa che il centro trapianti e il paziente condividono informazioni aggiornate con OPTN, che ha il potenziale per accelerare ilreneprocesso di assegnazione e quindi ridurre il tempo di ischemia fredda (CIT) e il tasso di eliminazione dei reni.
Le informazioni che possono essere condivise includono:
1. Soglia di accettazione del paziente k: Ogni paziente la segnalarenesoglia di accettazione della qualità k decisa da lei stessa e dal suo medico.
2. Eventuali criteri decisionali aggiuntivi utilizzati dal paziente: le decisioni del paziente e del chirurgo possono essere influenzate da informazioni non incluse nelrenevalutazione della qualità (KDPI). Avere parametri di qualità più standardizzati, in cui il paziente può prespecificare ciò che accetta, migliorerebbereneassegnazione. Con informazioni complete, OPTN potrebbe identificare istantaneamente i pazienti che accetterebbero il rene e risparmierebbero prezioso CIT.
3. La disponibilità attuale del paziente: un'indicazione aggiornata di se il paziente può attualmente ricevere il trapianto. I fattori includono la salute attuale e i viaggi.
4. Disponibilità del centro trapianti: considera la disponibilità del centro trapianti, ci sono strutture come sale operatorie preparate, chirurghi, infermieri e personale per eseguire l'intervento in tempo.
In condizioni di perfetta informazione, OPTN avrebbe accesso a informazioni aggiornate sulle soglie di accettazione di tutti i pazienti k, eventuali requisiti aggiuntivi per l'organo e se il paziente e il centro sono disponibili. Pertanto, OPTN potrebbe identificare direttamente il primo paziente in lista d'attesa che accetterà e riceverà il trapianto. Ciò ridurrà efficacemente la CIT, cioè t, al minimo necessario per estrarre l'organo ed eseguire il trapianto. Nel modello di simulazione, le informazioni perfette possono essere espresse impostando g sulla lunghezza della lista d'attesa, indicando che l'intera lista d'attesa viene cercata istantaneamente per un paziente corrispondente. Assumere informazioni perfette non è realistico per molte ragioni. Ad esempio, problemi tecnici possono influire sulla disponibilità delle informazioni e pazienti o centri potrebbero non mantenere tutte le informazioni costantemente aggiornate. Un'impostazione più realistica è migliorata ma la condivisione delle informazioni è ancora imperfetta. Maggiori informazioni significano che i pazienti possono essere identificati più velocemente utilizzando le informazioni condivise. Esprimiamo questo fatto nel modello di simulazione da un numero maggiore di pazienti che possono essere ricercati all'ora (cioè, un aumento di g).
Per illustrare l'effetto di una migliore condivisione delle informazioni, riportiamo i risultati per i pazienti di gruppo sanguigno A nella regione 6. Inizializziamo la lista d'attesa con 1000 pazienti ed eseguiamo la simulazione fino a quando la lunghezza della lista d'attesa non si stabilizza intorno a 1800 pazienti (200 mesi). Riportiamo i risultati dopo questo periodo di riscaldamento in media di oltre 300 mesi. La linea di base è la dimensione del gruppo attualmente utilizzata di g=5. Variamo g per rappresentare diversi livelli di condivisione delle informazioni.
La tabella 8 mostra l'impatto della condivisione delle informazioni espresso dal numero di pazienti in lista d'attesa che possono essere effettivamente presi in considerazione all'ora. Alla dimensione del gruppo di base di cinque, la qualità media del rene accettata è 0,66, portando a un'utilità media di 10,76 anni per paziente trapiantato. Il rene può viaggiare fino a 45 pazienti in lista d'attesa ed è accettato in media dal sesto paziente. La tabella 9 presenta l'utilizzo del rene e i tassi di mortalità in lista d'attesa, oltre al tasso di trapianto. Il tasso di utilizzo del rene aumenta significativamente all'aumentare di g.

Come mostra la Figura 5, il miglioramento delreneil tasso di trapianto è del 17% per il raddoppio della velocità del processo di offerta g=10 e raggiunge il 47% quando sono disponibili informazioni perfette. D'altra parte, il tasso di mortalità della lista d'attesa diminuisce del 7% quando g=10 e la riduzione può arrivare fino al 21%. La simulazione illustra l'effetto sull'efficienza che la condivisione delle informazioni può apportare al processo di allocazione.
La condivisione delle informazioni può essere implementata in molti modi, utilizzando la tecnologia attuale. Gli esempi includono l'utilizzo di app e dispositivi medici indossabili per monitorare la disponibilità del paziente quasi in tempo reale. Le interfacce standardizzate tra il sistema informativo dei centri trapianti e l'OPTN possono essere utilizzate per gestire la disponibilità del centro. L'implementazione di queste tecnologie richiederà tempo, ma i risultati presentati in questo studio di simulazione indicano che il potenziale guadagno è significativo con il potenziale di riduzionerenetassi di scarto al minimo.


5. Osservazioni conclusive
Il primo contributo di questa ricerca è lo sviluppo di un modello di simulazione che fornisce un donatore deceduto ottimalereneguida all'accettazione per i decisori (pazienti e chirurghi). La sfida principale della modellazione dell'accettazione/rigetto degli organi è incorporare condizioni e situazioni del mondo reale per prendere una decisione cruciale per salvare la vita. Per questo motivo, la nostra intenzione primaria come principale novità di questo lavoro è riconoscere, aggregare e implementare diversi elementi essenziali che contribuiscono ai criteri di selezione del rene. Il modello proposto tiene conto della diversità nella salute dei pazienti erenequalità, così come la loro correlazione. Inoltre, includiamo il deterioramento della qualità dei reni causato dall'accumulo di CIT durante il processo di assegnazione. Oltre a tutti gli elementi di cui sopra, incorporiamo anche la salute e la disponibilità del paziente insieme alle risorse umane e della struttura per proporre una soluzione di trapianto ottimale.
Il modello proposto può essere utilizzato per studiare come diverse scelte politiche possono influenzare gli obiettivi strategici dichiarati da OTPN [16]. Lo abbiamo illustrato con due applicazioni. In primo luogo, abbiamo mostrato come il modello può essere applicato per informare le decisioni dei pazienti in merito all'arruolamento multiplo dati i vincoli di costo, distanza e qualità dell'assistenza. Sebbene l'elenco multiplo a breve termine possa porre sfide all'equità tra i pazienti in base alle risorse finanziarie, ha il potenziale per uniformare le disparità geografiche nell'accesso ai trapianti e quindi aumentare l'equità.
Una seconda illustrazione richiama l'attenzione sull'aspetto del benessere socialerenetrapianto piuttosto che concentrarsi sulla ricerca di una soluzione ottimale come considerato nella prima applicazione. Confrontiamo i risultati del benessere sociale (vale a dire, l'utilizzo del rene del donatore e l'utilità post-trapianto a livello di sistema) per diversi livelli di informazioni disponibili, che vanno da nessuna informazione a informazioni perfette. Una maggiore informazione porta a un'assegnazione più rapida dei reni e a una riduzione del tasso di eliminazione dei reni. L'aumento del tasso di trapianto migliora l'utilità del benessere sociale e riduce la durata del trapiantorenelista d'attesa del trapianto, tempo e tasso di mortalità. I responsabili politici possono utilizzare questi risultati per motivare il valore della moderna tecnologia dell'informazione per raccogliere le informazioni necessarie e mostrare l'importanza di progettare strutture di incentivi che incoraggino la condivisione tempestiva delle informazioni da parte di pazienti e centri. Ad esempio, la progettazione di un'applicazione di trapianto di organi per un dispositivo smartphone può fornire un modo sicuro, facile e veloce per inviare e aggiornare le informazioni richieste in modo tempestivo. Il decisore politico potrebbe voler stabilire una regola di base che tutti i pazienti e i centri trapianti devono seguire per ricevere le offerte. Ad esempio, utilizzando la tecnologia e il servizio dell'app obbligatori, i centri trapianti possono rivedere o verificare i dati inviati regolarmente (ad esempio, ogni giorno) dopo che la posizione di un paziente nella lista d'attesa ha superato una determinata soglia. Il modello proposto è abbastanza semplice e flessibile da essere facilmente adattato per studiare molti altri aspetti del processo di assegnazione del rene.
Author CSutributiSus:Gli autori hanno contribuito in egual modo a questo lavoro. Tutti gli autori hanno letto e accettato la versione pubblicata del manoscritto
Finanziareing:Questa ricerca non ha ricevuto finanziamenti esterni.
InstitutiSual Review Board Statement:Non applicabile.
Informed Consitt Statemitt:Non applicabile.
Data AvaI lability Statement:Il set di dati utilizzato in questa analisi può essere ottenuto tramite UNOS.
Conflicts of Interest:Gli autori non dichiarano alcun conflitto di interessi.

bodybuilding per le lunghe
References
1. Università della California San Francisco. IlReneProgetto—Creazione di un bioartificialeRenecome soluzione permanente all'insufficienza renale. Disponibile online: (accesso il 4 aprile 2020).
2. NazionaleReneFondazione. Statistiche sulla donazione di organi e sui trapianti. 2016. Disponibile online: (accesso il 16 aprile 2020).
3. Regioni UNOS: Risorse regionali per il trapianto di organi. Disponibile online: (accesso il 20 marzo 2020).
4. OPTN. Politiche in vigore dal 6 dicembre 2020 [Ex Comm 9.9.A.]. Disponibile online: (accesso il 2 gennaio 2021).
5. Wey, A.; Salkowski, N.; Kasiske, BL; israeliano, AK; Snyder, JJ Influenza direnecomportamento di accettazione dell'offerta su metriche di efficienza di allocazione. Clin. Trapianto. 2017, 31, e13057.
6. Koizumi, N.; DasGupta, D.; Patel, AV; Smith, TE; Mayer, JD; Callender, C.; Melancon, JK Geographic Variation in Cold Ischemia Time:ReneVersus trapianto di fegato negli Stati Uniti, dal 2003 al 2011. Trapianto. Diretto2015, 1, e27.
7. Howard, DH Perché i chirurghi trapianti rifiutano gli organi?: Un modello della decisione di accettare/rifiutare. J. Economia sanitaria. 2002, 21, 957–969.
8. Lawson, C.; Johnson, D.; Clapper, D.; Fowler, K.; Kapur, S. Diminuendo ilReneTasso di scarto. Notizie sui reni. 2017. Disponibile online:(accesso il 22 febbraio 2020).
9. Zhang, J. Il suono del silenzio: apprendimento osservazionale negli Stati Unitirenemercato. Segno. Sci. 2010, 29, 315–335.
10. Schold, JD; Buccini, L.; Srinivas, T.; Srinivas, R.; Poggio, E.; Flechner, S.; Soria, C.; Segev, D.; Fung, J.; Goldfarb, D. L'associazione delle valutazioni delle prestazioni del centro erenevolume di trapianto negli Stati Uniti. Sono. J. Trapianto. 2013, 13, 67–75.
11. Schold, J.; Buccini, L.; Poggio, E.; Flechner, S.; Goldfarb, D. Association of Candidate Removals from theReneLista d'attesa del trapianto e supervisione delle prestazioni del centro. Sono. J. Trapianto. Spento. Marmellata. soc. Trapianto. Sono. soc. trasp. Surg. 2016, 16, 1276–1284.
12. Bae, S.; Massie, AB; Luo, X.; Anjum, S.; Desai, Nuovo Messico; Segev, DL Cambiamenti nel tasso di scarto dopo l'introduzione del Kidney Donor Profile Index (KDPI). Sono. J. Trapianto. 2016, 16, 2202–2207.
13. Schold, JD; Buccini, LD; Goldfarb, DA; Flechner, SM; Poggio, ED; Sehgal, AR Associazione trareneprestazioni del centro trapianti e beneficio in termini di sopravvivenza del trapianto rispetto alla dialisi. Clin. Marmellata. soc. nefrolo. 2014, 9, 1773–1780.
14. Haller, MC; Kainz, A.; Baer, H.; Oberbauer, R. L'annata della dialisi e gli esiti doporenetrapianto: uno studio di coorte retrospettivo. Clin. Marmellata. soc. nefrolo. 2016, 12, 122–130.
15. UNOS. Parlando di trapianto: domande frequenti su annunci multipli e trasferimento del tempo di attesa. 2017. Disponibile online: (accesso il 13 giugno 2020).
16. OPTN. Piano strategico OPTN/UNOS 2018–2021. Disponibile online: (accesso il 12 aprile 2020).
17. Chakkera, HA; Chertow, GM; O'Hare, AM; Modifica, WJ; Gonwa, TA Variazione regionale inreneesiti del trapianto: andamento nel tempo. Clin. Marmellata. soc. nefrolo. 2009, 4, 152–159.
18. Ardekani, SM; Orlowski, JM Elenco multiplo inrenetrapianto. Sono. J.ReneDis. 2010, 55, 717–725.
19. UNOS. Elenco multiplo. Disponibile online:(accesso il 1 dicembre 2018).
20. Gharibi, Z.; Ayvaci, MU; Hahsler, M.; Giacoma, T.; Gaston, RS; Tanriover, B. Rapporto costo-efficacia della terapia di induzione basata su anticorpi nel donatore decedutorenetrapianto negli Stati Uniti. Trapianto 2017, 101, 1234.






