Analisi morfologiche dell'espressione della nefrina nella glomerulonefropatia progressiva
Mar 25, 2022
Contatto:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Astratto:
In questo studio, ci siamo concentrati sulla nefrina, una delle molecole chiave all'interno del diaframma a fessura dei podociti, poiché sebbene ci siano state segnalazioni sulla sua espressione nell'uomo e nei ratti, la loro presenza negli uistitì comuni non è stata segnalata. Abbiamo studiato l'espressione della nefrina e i cambiamenti nei glomeruli, a seconda dello sviluppo della glomerulonefropatia progressiva spontanea negli uistitì comuni. Sono stati valutati diciannove uistitì comuni di età compresa tra due e dieci anni. Il rene è stato esaminato al microscopio con ematossilina ed eosina e colorazione immunoistochimica per la nefrina. Le lesioni sono state classificate in tre gradi secondo un sistema di classificazione delle lesioni renali riportato in precedenza. L'area nefrina-positiva è stata misurata mediante analisi morfometrica ed è stato calcolato il rapporto nefrina-positivo. L'espressione di nefrina è stata osservata lungo l'ansa capillare glomerulare con un pattern lineare continuo nei gradi di lesione renale da 0 a 2 e un pattern discontinuo lineare o granulare grossolano nel grado 3. L'espressione di nefrina tendeva a diminuire in modo significativo a seconda del grado delle lesioni renali . È stato suggerito che l'alterazione dell'espressione della nefrina svolga un ruolo importante nella progressione delle lesioni renali.
Parole chiave:nefrina, uistitì,glomerulonefropatia, rene, patologia

benefici del cistance del desertoePianta di Cistancheva bene perrene
introduzione
È noto che la glomerulonefropatia progressiva spontanea negli uistitì comuni (Callithrix jacchus) si manifesta frequentemente a partire dai due anni, con gravità della lesione che progredisce con l'età. In precedenza abbiamo riportato lesioni primarie e progressive di nefropatia in comuni uistitì1. Le alterazioni glomerulari primarie della nefropatia allo stadio iniziale sono caratterizzate dall'annullamento dei processi podocitari del piede e dall'ispessimento parziale della membrana basale glomerulare, che si presume causino fuoriuscita di proteine dai glomeruli, e possono essere osservate mediante ultramicroscopia ma non mediante microscopia ottica1–3. Inoltre, l'immunoglobulina svolge un ruolo importante nella progressione della nefropatia1, 2. Le IgM si depositano sul mesangio nella fase iniziale della glomerulonefropatia e, dopo la prima deposizione di IgM, l'area di deposito si espande all'intero glomerulo e le IgA e le IgG sono depositato con progressione2. I calchi ialini che suggeriscono la perdita di proteine dai glomeruli possono essere osservati al microscopio ottico con la progressione della glomerulonefropatia4. La proteinuria esacerba la progressione delle lesioni tubulo-interstiziali negli uistitì comuni4, come nell'uomo5, 6, e, in un recente studio sui glomeruli, la proteinuria potrebbe essere indotta da disturbi del diaframma a fessura, collegando così i processi adiacenti del piede (pedicelli) del podocita. Il diaframma a fessura è un complesso giunzionale intercellulare presente tra i processi del piede adiacenti e sono state identificate alcune molecole legate alla sua formazione3. Si pensava che una diminuzione dell'espressione di queste molecole o una disfunzione del diaframma a fessura fosse correlata alla progressione della proteinuria3. La nefrina, una delle molecole chiave espresse nel diaframma a fessura dei podociti, è una glicoproteina composta da 1241 aminoacidi ed è un noto biomarcatore utilizzato per monitorare il disturbo dei diaframmi a fessura7–10. Le molecole correlate ai diaframmi a fessura non sono state studiate nella nefropatia degli uistitì comuni, sebbene sia noto che in essi si verificano l'alterazione dei processi del piede dei podociti e la progressione della proteinuria. Inoltre, ci sono state segnalazioni sull'espressione della nefrina nell'uomo e nei ratti7-12 ma non negli uistitì. Pertanto, abbiamo studiato l'espressione della nefrina nei glomeruli e i cambiamenti nell'espressione della nefrina, a seconda della progressione della lesione, mediante analisi immunoistochimiche.

cistanche tcm
Materiali e metodi
Animali
Questo studio è stato approvato dal Comitato istituzionale per la cura e l'uso degli animali dell'Istituto centrale per gli animali sperimentali (CIEA; Kawasaki, Giappone) ed è stato condotto in stretta conformità con il regolamento per la sperimentazione animale della CIEA sulla base delle Linee guida per una corretta condotta di Esperimenti sugli animali (Consiglio scientifico del Giappone, 2006). Sono stati valutati diciannove uistitì comuni (11 maschi e 8 femmine) di CLEA Japan Inc. (Tokyo, Giappone). La loro età variava da 2 a 10 anni al momento dell'autopsia. Gli animali sono stati alloggiati in gabbie in una stanza per animali mantenuta ad una temperatura di 26 ± 3 gradi e un'umidità del 55 ± 20 per cento. Sono stati alimentati con LCMS-1M (CLEA Japan Inc., Tokyo, Giappone) e acqua del rubinetto. Gli animali sono stati sacrificati umanamente in anestesia con pentobarbital sodico per varie cause di moribondi (come la sintessi, la curvatura delle vertebre lombari, la lussazione dell'articolazione mandibolare, ecc.). L'analisi delle urine non è stata eseguita perché non è stato possibile eseguire il campionamento dell'urina.
Istopatologia
Ilrenisono stati perfusi con soluzione fisiologica, seguita da paraformaldeide al 4% e quindi fissati in formalina tamponata neutra al 10% per l'esame microscopico. I campioni sono stati incorporati in paraffina, sezionati con uno spessore di 5 μm e colorati con ematossilina ed eosina (HE). Le lesioni sono state classificate come lesioni glomerulari, tubulari e interstiziali sulla base dei criteri pubblicati1. I gradi di nefropatia sono stati divisi in quattro gruppi: grado 1 (3 maschi e 1 femmina), grado 2 (3 maschi e 5 femmine), grado 3 (1 maschio e 3 femmine) e grado 4 (3 maschi) (Tabella 1).

Per l'immunoistochimica, un anticorpo monoclonale contro il dominio extracellulare di origine umananefrina(1:1,000, Nefrinag{{0}}, Santa Cruz Biotechnology, Inc., Dallas, TX, USA) è stato utilizzato come anticorpo primario. Le sezioni di 5-μm sono state deparaffinate, reidratate, trattate con perossido di idrogeno al 3% a temperatura ambiente per 5 minuti e quindi riscaldate in autoclave a 121 gradi per 20 minuti in una soluzione di recupero target (pH 6,0, Dako, Glostrup, Danimarca). Dopo il raffreddamento, le sezioni sono state incubate con l'anticorpo primario a 4 gradi durante la notte. Il polimero IgG anti-topo e anti-coniglio coniugato con perossidasi (Histofine Simple Stain Rat MAX-PO(MULTI), Nichirei Bioscience Inc., Tokyo, Giappone) è stato utilizzato come anticorpo secondario per il metodo a base di polimeri13. Le sezioni sono state incubate con l'anticorpo polimerico secondario a temperatura ambiente per 30 minuti e i prodotti reagenti sono stati visualizzati utilizzando 3,3'-diamminobenzidina come cromogeno. La colorazione di contrasto è stata eseguita con ematossilina. Per il controllo negativo, l'anticorpo primario è stato omesso.
Analisi morfologica
Per l'analisi morfologica, i glomeruli con l'ilo glomerulare sono stati sottoposti all'esame e sono stati catturati da 16 a 28 glomeruli su ciascun vetrino (Tabella 1) utilizzando uno scanner per vetrini interi (Aperio AT2, Leica Microsystems Inc., Buffalo Grove, IL, USA) e un corrispondente software di visualizzazione di diapositive di patologia (Aperio ImageScope, Leica Microsystems Inc.) alla stessa risoluzione e dimensione dell'immagine.Nefrina-Le aree glomerulari positive e intere sono state calcolate con un software di analisi delle immagini (Image-Pro V10, Mediacybenetics Inc., Rockville MD, USA) disegnando una regione di interesse attorno al glomerulo, secondo un precedente rapporto14. Tutta l'area glomerulare è stata definita come l'area che si può distinguere dal fondo di colore bianco. Le soglie di colore per il calcolonefrina-le aree positive sono state determinate in base a ciascuna condizione di colorazione. Le soglie per rosso, verde e blu erano rispettivamente 37–67, 31–77 e 32–88. Il rapporto nefrina-positivo è stato calcolato dividendo le misurazioni delnefrina-area positiva sopra l'area glomerulare. L'analisi statistica è stata eseguita utilizzando il test di Jonckheere (livello di significatività: 5 percento, test unilaterale) per valutare l'andamento tra il grado di nefropatia e l'espressione dinefrina.

costa
Risultati
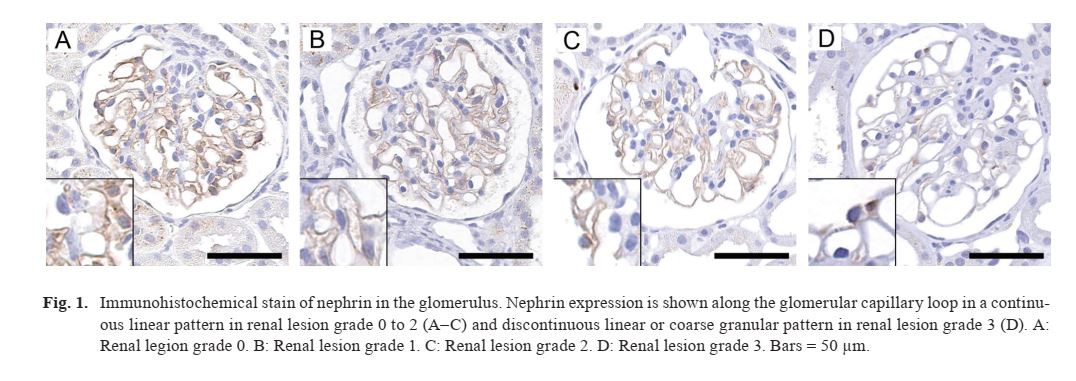
I punteggi patologici ei gradi delle singole lesioni renali sono mostrati nella Tabella 1. Come riportato nel nostro primo report1, il grado della lesione tendeva ad aumentare con l'età e non vi era alcuna evidente differenza di sesso. I risultati della colorazione immunoistochimica dinefrinasono mostrati in Fig. 1, e ilnefrina- il rapporto positivo è mostrato in Fig. 2 e Tabella 1. Tra i punteggi e i gradi nella Tabella 1, il grado della lesione renale, derivato dal punteggio totale di ciascuna lesione renale, e il punteggio del cast ialino sono stati utilizzati per il confronto con ilnefrina-rapporto positivo (Fig. 2 e 3). I singoli casi nella Tabella 1 sono mostrati in ordine crescente di grado di lesione renale. L'espressione della nefrina è stata osservata insieme all'ansa capillare glomerulare in uno schema lineare continuo nei gradi da 0 a 2 (Fig. 1A-C) e uno schema granulare discontinuo lineare o grossolano nei gradi 3 (Fig. 1D). Nel campione di controllo negativo, nessuna reazione positiva pernefrinaè stato osservato in qualsiasi sito.
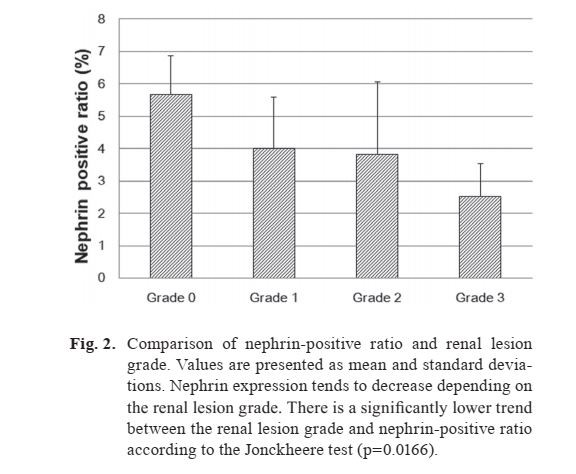
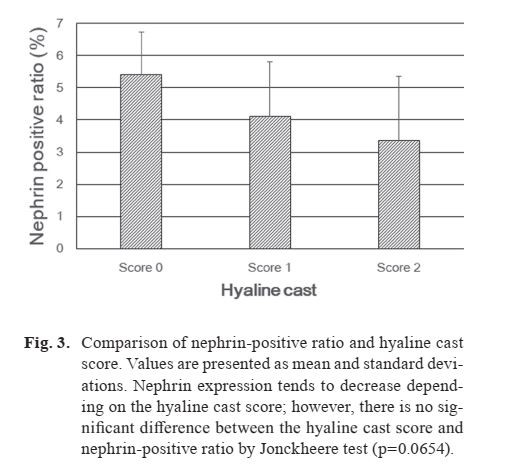
Il confronto delnefrina-rapporto positivo rispetto al grado della lesione renale è mostrato in Fig. 2. Nei casi di lesione renale di grado 0, la media ± deviazione standard (DS) delnefrina- il rapporto positivo era 5,66 ± 1,18 percento e i valori massimo, minimo e mediano erano rispettivamente 6,84 percento, 4,27 percento e 5,76 percento. Nei casi di grado 1, la media ± DS era 3,99 ± 1,61 percento e i valori massimo, minimo e mediano erano rispettivamente 5,69 percento, 1,19 percento e 4,35 percento. Nei casi di grado 2, la media ± DS era 3,82 ± 2,25 percento e i valori massimo, minimo e mediano erano rispettivamente 6,71 percento, 1,58 percento e 3,49 percento. Nei casi di grado 3, la media ± DS era 2,52 ± 1.02 percento e i valori massimo, minimo e mediano erano rispettivamente 3,67 percento, 2,17 percento e 2,17 percento. Collettivamente, le differenze individuali nell'espressione della nefrina erano piccole nei casi di grado 0, ma grandi nei casi di grado 1 o superiore e sporadicamente è stata rilevata una bassa espressione positiva.Nefrinal'espressione tendeva a diminuire a seconda del grado delle lesioni renali (Fig. 2). C'era una tendenza significativamente più bassa tra il grado di lesione renale enefrina-rapporto positivo secondo il test di Jonckheere (p=0.0166). Il punteggio del cast ialino rispetto al grado della lesione renale è mostrato in Fig. 3. Nei casi con un punteggio del cast ialino di 0, la media ± DS del rapporto positivo per nefrina era 5,40 ± 1,32 percento, nei casi con punteggio 1 era 4,10 ± 1,70 percento e, nei casi con punteggio 2, era 3,37 ± 1,98 percento. Secondo il test di Jonckheere (p=0.0654), si è verificata una tendenza significativamente più bassa tra il punteggio del cast ialino e il rapporto di positività alla nefrina.
Discussione
Una diminuzione della nefrina era correlata alla progressione delle lesioni renali durante lo sviluppo della glomerulonefropatia dell'uistitì. L'anticorpo anti-nefrina utilizzato in questo studio ha riconosciuto il dominio extracellulare sul lato N-terminale. Questo dominio extracellulare interagisce con le molecole NEPH1 e forma una struttura a cerniera all'interno del diaframma a fessura15. La localizzazione della nefrina nei glomeruli normali è lungo l'ansa capillare glomerulare e il pattern di colorazione è un pattern lineare di granuli fini continui sia nei ratti che nell'uomo11, 12, 16–18. La colorazione eseguita in questo studio è appropriata; ciò è confermato dall'osservazione che le pareti capillari a contatto con la regione mesangiale non erano macchiate, mentre lo erano quelle a contatto con i podociti. In condizioni anormali, come la sindrome nefrosica nell'uomo o la nefrosi con puromicina aminonucleoside nei ratti, il pattern di colorazione della nefrina nei glomeruli è discontinuo e granulare grossolano e l'intensità della colorazione immunoistochimica è più debole rispetto ai glomeruli normali11, 16, 17. Nel presente studio , il pattern di espressione della nefrina nei gradi da 0 a 2 era normale; tuttavia, il pattern di colorazione nei gradi 3 era paragonabile a quello delle condizioni anormali. In una precedente indagine sull'espressione della nefrina glomerulare in Crl: ratti CD(SD) con malattia a cambiamento minimo, l'espressione della nefrina era intatta, sebbene i processi del piede dei podociti mostrassero cancellazioni al microscopio elettronico senza apparenti cambiamenti morfologici osservati al microscopio ottico18. Nella malattia renale comune dei ratti, la nefropatia cronica progressiva (CPN), è stato dimostrato che l'albuminuria accompagnata da una CPN allo stadio iniziale può determinare un minor numero di alterazioni della permeabilità glomerulare dovute al mancato riassorbimento dell'albumina dai tubuli prossimali19. Nell'uomo, ci sono state alcune indagini sulla riduzione dell'espressione della nefrina in presenza di modifiche minori10 o in altre malattie renali14, 16. D'altra parte, è stato riportato un rapporto sull'espressione di nefrina intatta nella nefrosi a modificazioni minime20. La presenza o l'assenza di un cambiamento nell'espressione della nefrina nella malattia nefrosica a cambiamento minimo è ancora in discussione. In realtà, era difficile confermare l'aumento o la diminuzione della reazione anticorpale della nefrina mediante l'osservazione visiva nella nefropatia dell'uistitì, ma è stato possibile rilevare il cambiamento nell'intero rene mediante l'analisi dell'immagine. La nostra indagine suggerisce che l'anomalia dei diaframmi a fessura del glomerulo può essere coinvolta nella progressione della nefropatia negli uistitì comuni a causa di una diminuzione della nefrina. La trasformazione del pattern di colorazione positivo della nefrina, da lineare a granulare, è stata riportata in un modello animale di ratto di malattia nefrosica durante lo sviluppo della lesione11, 16, 21. Un'associazione tra anomalie della membrana della fessura e proteinuria è stata stato segnalato frequentemente22, 23; pertanto, è stato ipotizzato che la proteinuria possa essere causata da una disfunzione del diaframma a fessura. Nel nostro studio sulla nefropatia dell'uistitì, la progressione della permeabilità alle proteine glomerulari dovuta alla disfunzione del diaframma a fessura potrebbe essersi verificata perché le caratteristiche morfologiche dei calchi ialini sono state osservate solo nei casi senza alterazioni tubulo-interstiziali. In questo studio, non è stata osservata alcuna differenza statisticamente significativa tra il punteggio dei cambiamenti morfologici dei cilindri ialini e la diminuzione dell'espressione della nefrina. Tuttavia, l'espressione della nefrina tende a diminuire a seconda del punteggio del cast ialino, che è un indicatore della perdita di proteine dal glomerulo.
Nella nostra precedente indagine, è stata osservata la cancellazione dei processi del piede nella fase iniziale della nefropatia dell'uistitì e l'area del processo del piede interessata è stata espansa a seconda del grado della lesione renale1. La tabella 2 mostra la relazione tra il tasso di riduzione della nefrina in questo studio e i risultati della microscopia elettronica per ciascun grado di lesione renale da uno studio precedente. Si ritiene che l'annullamento sia dovuto a una rottura del citoscheletro di actina dei processi del piede24. La nefrina viene defosforilata quando viene costruita la membrana a fessura e si lega all'actina attraverso CD2AP e podocina25, 26. Quando un diaframma a fessura viene danneggiato, le molecole di nefrina si raggruppano, inducendo la fosforilazione della nefrina, la polimerizzazione dell'actina e l'annullamento dei processi del piede26. La fosforilazione della nefrina si verifica anche rapidamente in seguito all'induzione dell'annullamento del processo del piede nel modello di solfato di protamina nei topi27. La nefrina è una proteina di adesione glomerulare associata alla maturazione, differenziazione, formazione del processo e segnalazione dei podociti24. La nostra indagine ha mostrato che esisteva una correlazione tra la riduzione dell'espressione della nefrina, determinata dall'immunoistochimica, e la progressione del grado della lesione renale, suggerendo un'espansione dell'eliminazione dei processi del piede podocita. Tuttavia, non è chiaro se le anomalie nel complesso proteico del diaframma a fessura causino danni ai processi del piede dei podociti o se il danno ai podociti causi cambiamenti nei diaframmi a fessura e riduzione della nefrina. Poiché la nefrina è anche coinvolta nella differenziazione dei podociti, si pensa che questa relazione sarà ulteriormente chiarita dai dati sulla rigenerazione e differenziazione dei podociti.

In conclusione, i nostri risultati forniscono informazioni sunefrinaespressione nella glomerulonefropatia progressiva negli uistitì comuni. L'analisi morfologica ha evidenziato un andamento inferiore dinefrinal'espressione nei podociti nella glomerulonefropatia progressiva dell'uistitì comune e l'alterazione dinefrinal'espressione è stata suggerita per svolgere un ruolo importante nella progressione delle lesioni renali.
Divulgazione di potenziali conflitti di interesse:
Gli autori dichiarano di non avere conflitti di interesse.
Riconoscimento:
Gli autori desiderano ringraziare il Sig. Takayoshi Ito per l'eccellente assistenza tecnica fornita. Gli autori ringraziano anche la Sig.ra Kanae Tamatsukuri e il Sig. James Harada per l'editing linguistico del manoscritto.
sistano
Riferimenti
1. Yamada N, Sato J, Kanno T, Wako Y e Tsuchitani M. Studio morfologico della glomerulonefropatia progressiva negli uistitì comuni (Callithrix jacchus). Patolo tossicologico. 41: 1106–1115. 2013.
2. Yamada N, Hashimoto N, Kamiie J, Doi T, Sato J, Inoue T, Shirota K e Tsuchitani M. Relazione tra deposizione di immunoglobuline e lesioni precoci della glomerulonefropatia progressiva nei giovani uistitì comuni. Vet Pathol. 55: 173–176. 2018.
3. Cara-Fuentes G, Clapp WL, Johnson RJ e Garin EH. Patogenesi della proteinuria nella malattia a cambiamenti minimi idiopatici: meccanismi molecolari. Nefrolo pediatrico. 31: 2179–2189. 2016.
4. Isobe K, Adachi K, Hayashi S, Ito T, Miyoshi A, Kato A e Suzuki M. Lesioni spontanee glomerulari e tubulo-interstiziali in uistitì comuni (Callithrix jacchus). Vet Pathol. 49: 839–845. 2012.
5. Eddy AA. Proteinuria e danno interstiziale. Trapianto di quadrante di nefrolo. 19: 277–281. 2004.
6. Hingorani S, Gooley T, Pao E, Sandmaier B e McDonald G. Citochine urinarie dopo HCT: evidenza di infiammazione renale nella patogenesi della proteinuria erenepatologia. Trapianto di midollo osseo. 49: 403–409. 2014.
7. Kestilä M, Lenkkeri U, Männikkö M, Lamerdin J, McCready P, Putaala H, Ruotsalainen V, Morita T, Nissinen M, Herva R, Kashtan CE, Peltonen L, Holmberg C, Olsen
A e Tryggvason K. Il gene clonato posizionalmente per una nuova proteina glomerulare--nefrina--è mutato nella sindrome nefrosica congenita. Mol Cell. 1: 575–582. 1998.
8. Langham RG, Kelly DJ, Cox AJ, Thomson NM, Holthöfer H, Zaoui P, Pinel N, Cordonnier DJ e Gilbert RE. Proteinuria ed espressione della proteina del diaframma a fessura del podocita, nefrina, nella nefropatia diabetica: effetti dell'inibizione dell'enzima di conversione dell'angiotensina. Diabetologia. 45: 572–1576. 2002.
9. Gallese GI e Saleem MA. Molecola caratteristica della nefrina del podocita glomerulare? J Pathol. 220: 328–337. 2010.
10. van de Lest NA, Zandbergen M, IJpelaar DHT, Wolterbeek R, Bruijn JA, Bajema IM e Scharpfenecker M. La perdita di nefrina può essere utilizzata per prevedere la remissione e l'esito renale a lungo termine nei pazienti con malattia a variazione minima.ReneRep. int. 3: 168–177. 2017.
11. Kawachi H, Koike H, Kurihara H, Yaoita E, Orikasa M, Shia MA, Sakai T, Yamamoto T, Salant DJ e Shimizu F. Clonazione di nefrina di ratto: espressione nello sviluppo dei glomeruli e negli stati proteinurici.Reneint. 57: 1949–1961. 2000.
12. Luimula P, Ahola H, Wang SX, Solin ML, Aaltonen P, Tikkanen I, Kerjaschki D e Holthöfer H. Nephrin nella malattia glomerulare sperimentale.Reneint. 58: 1461–1468. 2000.
13. Janardhan KS, Jensen H, Clayton NP e Herbert RA. Immunoistochimica nella patologia investigativa e tossicologica. Patolo tossicologico. 46: 488–510. 2018.
14. Koop K, Eikmans M, Baelde HJ, Kawachi H, De Heer E, Paul LC e Bruijn JA. Espressione di molecole associate a podociti nell'uomo acquisitorenemalattie. J Am Soc Nephrol. 14: 2063–2071. 2003.
15. Gerke P, Huber TB, Sellin L, Benzing T e Walz G. Omodimerizzazione ed eterodimerizzazione delle proteine dei podociti glomerulari nefrina e NEPH1. J Am Soc Nephrol. 14: 918–926. 2003.
16. Doublier S, Ruotsalainen V, Salvidio G, Lupia E, Biancone L, Conaldi PG, Reponen P, Tryggvason K e Camussi G. La ridistribuzione della nefrina sui podociti è un potenziale meccanismo di proteinuria nei pazienti con sindrome nefrosica acquisita primaria. Sono J Pathol. 158: 1723–1731. 2001.
17. Kawakami H, Kamiie J, Yasuno K, Kobayashi R, Aihara N e Shirota K. Dinamica della quantità assoluta di nefrina in un singolo podocita in ratti con puromicina aminonucleoside nefrosi calcolata mediante approccio proteomico glomerulare quantitativo con modalità di monitoraggio della reazione selezionata. Trapianto di quadrante di nefrolo. 27: 1324–1330. 2012.
18. Yasuno K, Honda K, Hakamata S, Kai K e Mori K. Malattia da cambiamento minimo delrenein un giovane topo Sprague Dawley. J Toxicol Pathol. 31: 55–59. 2018.
19. Obert LA e Frazier KS. Coinvolgimento del sistema renina-angiotensina intrarenale nella patogenesi della nefropatia cronica progressiva, colmando il divario informativo tra le discipline. Patolo tossicologico. 47: 799–816. 2019.
20. Patrakka J, Ruotsalainen V, Ketola I, Holmberg C, Heikinheimo M, Tryggvason K e Jalanko H. Espressione di nefrina in pediatriarenemalattie. J Am Soc Nephrol. 12: 289–296. 2001.
21. Saran AM, Yuan H, Takeuchi E, McLaughlin M e Salant DJ. Il complemento media la ridistribuzione della nefrina e la dissociazione dell'actina nella nefropatia membranosa sperimentale.Reneint. 64: 2072–2078. 2003.
22. Gagliardini E, Benigni A, Tomasoni S, Abbate M, Kalluri R e Remuzzi G. Sottoregolazione mirata della nefrina extracellulare nella nefropatia da IgA umana. Sono J Nephrol. 23: 277–286. 2003.
23. Wakamatsu A, Fukusumi Y, Hasegawa E, Tomita M, Watanabe T, Narita I e Kawachi H. Ruolo della calcineurina (CN) inrenepodocita glomerulare: l'inibitore del CN ha migliorato la proteinuria inibendo la ridistribuzione del CN al diaframma a fessura. Physiol Rep. 4: e12679. 2016.
24. Garg P. Una rassegna della biologia dei podociti. Sono J Nephrol. 47 (Suppl 1): 3–13. 2018.
25. Ichimura K, Kurihara H e Sakai T. Organizzazione del filamento di actina dei processi del piede nei podociti di ratto. J Histochem Cytochem. 51: 1589–1600. 2003.
26. Ronco P. Proteinuria: è tutto nel piede? JClin Invest. 117: 2079–2082. 2007.
27. Verma R, Kovari I, Soofi A, Nihalani D, Patrie K e Holzman LB. L'impegno dell'ectodominio della nefrina provoca l'attivazione della chinasi Src, la fosforilazione della nefrina, il reclutamento di Nck e la polimerizzazione dell'actina. JClin Invest. 116: 1346–1359. 2006.
